

| A、溶液中H+向负极移动 |
| B、电子由Zn经外电路流向Cu |
| C、Zn电极反应:Zn-2e-=Zn2+ |
| D、Cu是正极 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、向NaHSO4溶液中滴入Ba(OH)2溶液至中性H++SO42-+Ba2++OH═BaSO4↓+H2O |
| B、由水电离的c(H+)为10-3mol?L-1的溶液中,Na+、NO3-、SO32-、Cl-一定能大量共存 |
| C、向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总的物质的量为2mol |
| D、可以用浓盐酸酸化的KMnO4溶液与H2O2混合,以汪明H2O2具有还原性2MnO4+6H++5H2O2═2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、推进以防治PM2.5为重点的大气污染防治工作 |
| B、积极推广风能、太阳能、氢能等新型能源的使用 |
| C、将生活垃圾、废品分类,实现资源再循环 |
| D、将高能耗、高污染的企业迁至偏僻的农村地区,提高当地居民收入 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaClO3中Cl的化合价是+5 |
| B、被氧化的Cl原子和被还原的Cl原子的物质的量的比为1:5 |
| C、Cl2既是氧化剂又是还原剂 |
| D、每生成1mol的NaClO3转移6mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“红外眼睛”对热非常敏 |
| B、“红外眼睛”的热目标是敌机发动机或尾部喷口高温区 |
| C、“红外眼睛”的电阻值随温度明显变化 |
| D、“红外眼睛”的工作原理与人眼相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| ①B2H4 |
| ②H2O2/OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
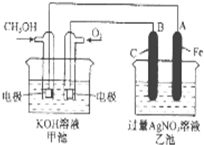 右图是一个化学过程的示意图.已知甲池的总反应式为:
右图是一个化学过程的示意图.已知甲池的总反应式为:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com