

| A、用图①所示实验装置排空气法收集H2气体 |
| B、图②装置可以用来验证化学能转化为电能 |
| C、图③铁片最终完全溶解,且高锰酸钾溶液褪色 |
| D、图④所示实验可比较硫、碳、硅三种元素的非金属性强弱 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用蒸发皿进行加热蒸发实验时,不垫石棉网 |
| B、浓硫酸不慎沾到皮肤上,迅速用NaOH溶液清洗,再用水洗 |
| C、蒸馏时,将温度计水银球插入液面以下 |
| D、闻气体气味时,用手在容器口轻轻扇动,使少量气体飘入鼻孔中 |
| E、使用分液漏斗和容量瓶时,首先检查是否漏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在25℃时,向弱酸HAc中逐滴滴人NaOH溶液,在不同的pH下,HAc分子与Ac-离子的含量如图所示,则下列说法正确的是( )
在25℃时,向弱酸HAc中逐滴滴人NaOH溶液,在不同的pH下,HAc分子与Ac-离子的含量如图所示,则下列说法正确的是( )| A、当pH<2.6时,HAc不电离 |
| B、O点时.HAc恰好与NaOH完全反应 |
| C、pH=6.4时溶液中溶质只有NaAc |
| D、50℃,曲线交点O点pH<4.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 实验Ⅰ:产生红褐色沉淀 |
B、 实验Ⅱ:试管中溶液变红色 |
C、 实验Ⅲ:试管中溶液变红色 实验Ⅲ:试管中溶液变红色 |
D、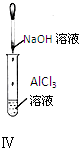 实验Ⅳ:试管中先出现白色沉淀,后溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| B、c(H+)=c(NH3?H2O)+c(OH-) |
| C、加水稀释,溶液中所有离子的浓度均减小 |
| D、向溶液中加入少量CH3COONa固体,NH4+的水解程度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 预期现象与结论 |
| 取少量反应后固体于试管中, | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com