下列叙述完全正确的一组是( )
①一定条件,气体的摩尔体积为11.2L
②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极放出0.2g H2,则电路中通过的电子数为0.2NA
③在标准状况下,11.2L NO与11.2L O2混合后的气体分子数为0.75NA
④常温常压下,16g O3所含的原子数为NA
⑤1mol C10H22分子中共价键总数为31NA
⑥氦气的摩尔质量为8g
⑦标准状况下,22,4L水中所含的分子数为NA.
A.①②③④⑤
B.②④⑤⑥⑦
C.②④⑤
D.①②⑤
【答案】
分析:①一定温度压强的气体气体摩尔体积一定,标准状况气体气体摩尔体积为22.4L/mol;
②依据原电池反应中 的电极反应和电子守恒计算;
③依据n=

计算物质的量结合反应化学方程式判断反应情况,生成的二氧化氮存在和四氧化二氮气体的平衡分析;
④元素守恒,计算氧原子数;
⑤依据烷烃分子结构计算化学键;
⑥氦气是单原子分子,摩尔质量单位是g/mol;
⑦标准状况水不是气体;
解答:解:①一定条件下,1mol气体的体积可以是11.2L,但气体摩尔体积的单位是L/mol;故①错误;
②铜锌原电池正极上生成0.1mol氢气,需要0.2mol电子.所以电路中 通过电子数0.2N
A,故②正确;
③NO和O
2反应生成NO
2,一氧化氮物质的量为0.5mol,O
2物质的量为0,5mol,反应后生成NO2物质的量为0.5mol,剩余O
2物质的量0.25mol,但存在2NO
2?N
2O
4的化学平衡,气体总分子数小于0.75N
A,故③错误;
④常温常压下,16g O
3所含的原子数=
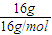
×N
A=N
A;故④正确;
⑤依据结构分析计算1mol C
10H
22分子中共价键总数=1mol(10-1+22)×N
A=31N
A,
⑥氦气是单原子分子其相对分子质量为4,摩尔质量4g/mol,故⑥错误;
⑦标准状况水不是气体,22.4L水不是1mol,故⑦错误;
故选C.
点评:本题考查了阿伏伽德罗常数的应用,主要是气体摩尔体积条件应用,原电池反应的电子转移计算,质量换算物质的量计算微粒数,注意气体摩尔体积的概念理解和稀有气体是单原子分子,题目难度中等.

 计算物质的量结合反应化学方程式判断反应情况,生成的二氧化氮存在和四氧化二氮气体的平衡分析;
计算物质的量结合反应化学方程式判断反应情况,生成的二氧化氮存在和四氧化二氮气体的平衡分析;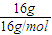 ×NA=NA;故④正确;
×NA=NA;故④正确;
