
 ��1�������ᣨH3PO3���Ƕ�Ԫ�ᣬ������NaOH��Һ��Ӧ������Na2HPO3�����Na2HPO3��Һ�ɵõ������ᣬװ��ʾ��ͼ���£�
��1�������ᣨH3PO3���Ƕ�Ԫ�ᣬ������NaOH��Һ��Ӧ������Na2HPO3�����Na2HPO3��Һ�ɵõ������ᣬװ��ʾ��ͼ���£����� ��1����������������������ʧ���ӷ���������Ӧ�������Ϸ����õ��ӵĻ�ԭ��Ӧ��
�ڲ�Ʒ����HPO32-�������ӽ�����������
��2����д��ȼ�ϵ�ص��ܷ�Ӧʽ����д�������ĵ缫��Ӧʽ������ø����缫��Ӧʽ������ÿ���缫ת�Ƶ�������ͬ�������ͭ��������
��� �⣺��1��������������������ʧ���ӷ���������Ӧ���缫��ӦʽΪ4OH--4e-=2H2O+O2���������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H++2e-=H2�����ʴ�Ϊ��2H++2e-=H2����
�ڲ�Ʒ����HPO32-�������ӽ�����������ᣬ��Ӧ���ӷ���ʽΪ��HPO32-+2H+=H3PO3���ʴ�Ϊ��HPO32-+2H+=H3PO3��
��2�������ѡ�������KOH��ҺΪԭ���ܵ�ط�Ӧ����ʽΪ��CH3OCH3+3O2+4OH-=2CO32-+5H2O ��
�����缫��ӦʽΪ��3O2+6H2O+2e-=12e- ��
��-�ڵã�CH3OCH3-12e-+16OH -=2CO32-+11H2O
n��CH3OCH3��=$\frac{1.12L/min��0.5min}{22.4L/mol}$=0.025mol
n��Cu2+��=0.5L��2mol/L=1mol
CH3OCH3��12e- Cu2+��2e-��Cu
1 12 2 64
0.025 0.3 0.3 9.6
�ʴ�Ϊ��CH3OCH3-12e-+16OH-=2CO32-+11H2O��9.6g��
���� ���⿼����ȼ�ϵ�ء����ؼ���֪ʶ��ע��֪ʶ�Ĺ��ɺ������ǹؼ����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢݢ� | B�� | �ڢܢݢޢ� | C�� | �٢ܢݢޢ� | D�� | �ڢۢܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� | 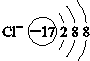 | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ���ҿ��ö����ЧӦ����������Һ | |
| B�� | �����ʺ硱����һ����Ȼ�������ǹ�ѧ����ͬʱҲ�뽺���й� | |
| C�� | ������1mol Fe��OH��3�Ľ����У�����NA��Fe��OH��3���� | |
| D�� | ��ɢ�����Ӵ�С����1��100nm֮��ķ�ɢϵ��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | һl30 | 9 | -1l6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com