

分析 (1)根据炔烃的命名原则写出4,4,5-三甲基-2-己炔的结构简式;
(2)对硝基甲苯是甲苯对位连接硝基取代基;
(3)2,2-二甲基-3-乙基壬烷:主链为壬烷,含有9个C,在2号C含有2个甲基、在3号C含有1个乙基.
解答 解:(1)4,4,5-三甲基-2-己炔,该有机物主链为己炔,碳碳三键在2号C,在4、4、5号C原则各含有1个甲基,该有机物的结构简式为CH3C≡C-C(CH3)2CH(CH3)2,故答案为:CH3C≡C-C(CH3)2CH(CH3)2;
(2)对硝基甲苯的结构简式为 ,故答案为:
,故答案为: ;
;
(3)2,2-二甲基-3-乙基壬烷:主链为壬烷,含有9个C,在2号C含有2个甲基、在3号C含有1个乙基,该有机物的结构简式为:CH3C(CH3)2CH(C2H5)CH2CH2CH2CH2CH2CH3,
故答案为:CH3C(CH3)2CH(C2H5)CH2CH2CH2CH2CH2CH3.
点评 本题考查了有机物的结构简式和键线式的书写,题目难度不大,一般要求了解烷烃的命名、苯的同系物的命名及简单的烃的衍生物的命名规则,据此即可写出结构简式.


科目:高中化学 来源: 题型:选择题
| A. | 用pH计测得某溶液的pH值为9.70 | |
| B. | 用25mL移液管移取19.50 mL的液体 | |
| C. | 用电子天平称取镀锌4.421g | |
| D. | 用25mL酸式滴定管量取16.50mLKMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单独利用焓变的数据或熵变的数据就能判断化学反应能否自发进行 | |
| B. | 在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 | |
| C. | 利用反应热数据的大小可以判断不同反应的反应速率的大小 | |
| D. | 利用溶液的pH与7的大小关系,可以判断任何温度下溶液的酸碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
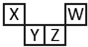 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y所形成的一种单质有毒且易自燃.下列判断不正确的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y所形成的一种单质有毒且易自燃.下列判断不正确的是( )| A. | 最高正化合价:X<Y<Z<W | |
| B. | 原子半径:W<Z<Y | |
| C. | 气态氢化物的热稳定性:Y<Z<W | |
| D. | 最高价氧化物对应水化物的酸性:X<Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
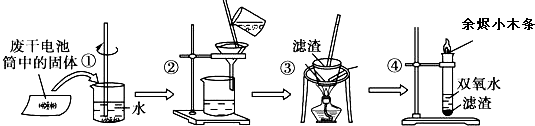
| A. | 步骤①的操作名称是溶解 | |
| B. | 步骤②中玻璃棒的作用是引流 | |
| C. | 步骤③的操作名称是蒸发 | |
| D. | 步骤④中的双氧水加入滤渣后迅速产生大量气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②③④ | C. | ①②③⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com