
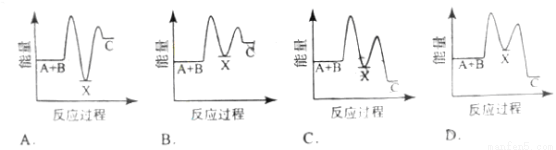
反应 A+B →C(△H <0)分两步进行 ① A+B→X (△H>0) ② X→C(△H <0)下列示意图中,能正确表示总反应过程中能量变化的是
科目:高中化学 来源:2014-2015学年河南省新郑市高一上学期期中学业水平测试化学试卷(解析版) 题型:填空题
(11分)(1)现有同温同压下的0.3mol SO2和0.2mol CO2 ,两者的质量比为 ;所含原子个数比为 ;密度比为 ;
(2)有一金属氯化物MCl2 27g , 含有0.40molCl-, 则该氯化物的物质的量为 , 其摩尔质量为 ,金属M的相对原子质量为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高一上学期期中考试化学试卷(解析版) 题型:选择题
新型纳米材料氧缺位铁酸盐(MFe2Ox)(3<x<4,M表示Mn、Co、Zn或Ni的二价离子),常温下,它能使工业废气中的SO2、NO2等氧化物转化为单质。转化流程如图所示:
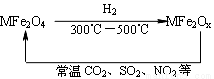
有关上述转化过程的下列叙述正确的是
A.MFe2O4表现了还原性
B.MFe2Ox表现了还原性
C.SO2和NO2表现了还原性
D.SO2和NO2发生了分解反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高二10月月考化学试卷(解析版) 题型:填空题
(16分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1NaOH溶液,实验尚缺少的玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
实验用品 | 溶液温度 | 中和热 | |||
t1 | t2 | ΔH | |||
① | 50 mL 0.55 mol·L-1 NaOH溶液 | 50 mL 0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.3 ℃ |
|
② | 50 mL 0.55 mol·L-1 NaOH溶液 | 50 mL 0.5 mol·L-1 HCl溶液 | 20 ℃ | 23.5 ℃ | |
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。
①计算完成上表。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高二10月月考化学试卷(解析版) 题型:选择题
已知火箭燃料二甲基肼(CH3—NH—NH—CH3)的燃烧热为-6 000 kJ·mol-1,则30 g二甲基肼完全燃烧放出的热量为
A.3000 kJ B.1500 KJ C.6 000 kJ D.12 000 kJ
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高二10月月考化学试卷(解析版) 题型:选择题
下列反应属于吸热反应的是
A.炭燃烧生成一氧化碳
B.中和反应
C.锌粒与稀硫酸反应制取H2
D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省英文学校高一10月月考化学试卷(解析版) 题型:填空题
(10分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解法 C.结晶法 D.分液法
E.蒸馏法 F.过滤法
(1)分离饱和食盐水与沙子的混合物________。
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾________。
(3)分离水和汽油的混合物________。
(4)分离四氯化碳(沸点为76.6℃)和甲苯(沸点为110.6℃)的混合物________。
(5)从碘的水溶液里提取碘________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省南阳市上学期10月月考高二化学试卷(解析版) 题型:填空题
Ag2O2是银锌碱性电池的正极活性物质,可通过下列方法制备:在KOH加入适量AgNO3 溶液,生成Ag2O沉淀,保持反应温度为80,边搅拌边将一定量K2S2O8溶液缓慢加到上述混合物中,反应完全后,过滤、洗涤、真空干燥得到固体样品.反应方程式为
2AgNO3+4KOH+K2S2O8 Ag2O2↓+2KNO3+2K2SO4+2H2O
Ag2O2↓+2KNO3+2K2SO4+2H2O
回答下列问题:
(1)上述制备过程中,检验洗剂是否完全的方法是
(2)银锌碱性电池的电解质溶液为KOH溶液,电池放电时正极的Ag2O2 转化为Ag,负极的Zn转化为K2Zn(OH)4,写出该电池反应方程式: .
(3)准确称取上述制备的样品(设仅含Ag2O2和Ag2O) 2.558g,在一定的条件下完全分解为Ag 和O2,得到224.0mLO2(标准状况下).计算样品中Ag2O2的质量分数(计算结果精确到小数点后两位).
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高二上第一次月考化学(解析版) 题型:选择题
在一定温度下,在一个密闭容器中加入H2和I2蒸气各0.5mol,发生反应H2+I2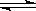 2HI,达到平衡时,生成HI 0.8 mol,若其它条件不变,开始充入的H2为2 mol,则达到平衡时生成的HI可能是下列中的
2HI,达到平衡时,生成HI 0.8 mol,若其它条件不变,开始充入的H2为2 mol,则达到平衡时生成的HI可能是下列中的
A 1.1 mol B 0.87 mol C 0.8 mol D 0.5 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com