
���� W��V��X��Y��Z��ԭ���������εݼ������ֳ���Ԫ�أ�XԪ���ǵؿ��к�������Ԫ�أ���XΪOԪ�أ�Y��Z��ɵ���̬������M��ˮ��Һ�ʼ��ԣ�����֪YΪNԪ�ء�ZΪHԪ�أ�MΪNH3��V�ĵ�����X2��ȼ�ղ����ʹƷ����Һ��ɫ������֪VΪSԪ�أ�W��һ����ʷ�ƾá�Ӧ����㷺�Ľ���Ԫ�أ���WΪFeԪ�أ��ݴ˽��
��� �⣺W��V��X��Y��Z��ԭ���������εݼ������ֳ���Ԫ�أ�XԪ���ǵؿ��к�������Ԫ�أ���XΪOԪ�أ�Y��Z��ɵ���̬������M��ˮ��Һ�ʼ��ԣ�����֪YΪNԪ�ء�ZΪHԪ�أ�MΪNH3��V�ĵ�����X2��ȼ�ղ����ʹƷ����Һ��ɫ������֪VΪSԪ�أ�W��һ����ʷ�ƾá�Ӧ����㷺�Ľ���Ԫ�أ���WΪFeԪ�أ�
��1��YΪNԪ�أ������ڱ��е�λ���ǣ��ڶ����ڵڢ�A�壻ΪH2O2��������H2O2������������������������Ư����
�ʴ�Ϊ���ڶ����ڵڢ�A�壻����������������Ư����
��2��O��N��H����Ԫ�ؿ����һ��ǿ��UΪHNO3���������ʵ������±�HNO3��������NH4NO3�����ε�ˮ��Һ��NH4+����ˮ�⣺NH4++H2O?NH3��H2O+H+���ƻ�ˮ�ĵ���ƽ�⣬��Һ�����ԣ���ҺpHС��7��
�ʴ�Ϊ��С�ڣ�
��3����FeͶ�뵽������Һ�У�������dz��ɫFeCl2��Һ��˫��ˮ����ǿ�����ԣ����������½�������������Ϊ�����ӣ�ͬʱ����ˮ��FeCl2��������Һ��˫��ˮ��Ӧ�����ӷ���ʽΪ2Fe2++2H++H2O2=2Fe3++2H2O��
����������Ԫ������������γɵĻ������У���һ����������ˮ��Ӧ���������ҷ�Ӧ����������ԭ��Ӧ��Ӧ�Ƕ���������ˮ��Ӧ����������NO���÷�Ӧ�Ļ�ѧ����ʽΪ��3NO2+H2O=2HNO3+NO��
�ʴ�Ϊ��2Fe2++2H++H2O2=2Fe3++2H2O��3NO2+H2O=2HNO3+NO��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã���Ŀ�Ѷ��еȣ��ƶ�Ԫ�ص������ǹؼ���ע���Ԫ�ػ��������ʵ����գ�


 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���ᷴӦ��2Fe+6H+�T2Fe3++3H2�� | |
| B�� | ����FeCl3��Һ��Ӧ��Fe+Fe3+�T2Fe2+ | |
| C�� | �ƺ���ˮ��Ӧ��2Na+2H2O=�T2Na++2OH-+H2�� | |
| D�� | FeCl2��Һ��Cl2��Ӧ��Fe2++Cl2�TFe3++2Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
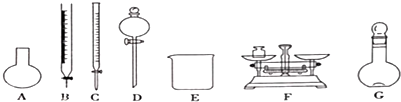
| A�� | ��Ҫ����NaClO���������Ϊ144.0g | |
| B�� | ����ҡ�Ⱥ�����ҺҺ���������ƿ�̶��ߣ������ټ�ˮ���� | |
| C�� | ������ͼ��ʾ��������ѡ����Ҫ�����⣮��-�ֲ������� | |
| D�� | ����ƿ������ˮϴ����Ӧ��ɲ���������Һ���ƣ���t���ƫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ˮ | B�� | �����ȥ���� | C�� | ʳ����ϴˮ�� | D�� | ���������;� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ������ȡO2��ʵ������ȡH2 | B�� | ʵ������ȡCO2��CO2ͨ��ʯ��ˮ�� | ||
| C�� | ʵ���ҵ��ˮ��CaO����ˮ | D�� | �⡢��������屬��������ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
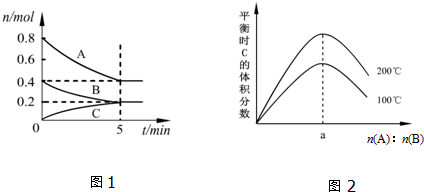
| A�� | 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v��B��=0.04 mol•L-1•min-1 | |
| B�� | ͼ2��֪��ӦxA��g��+yB��g��?zC��g���ġ�H��0����a=2 | |
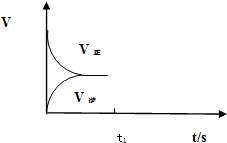
| C�� | ����ͼ1��ʾ��ƽ��״̬�£�������ϵ�г���He����ʱv����v�� | |
| D�� | 200��ʱ���������г���1.6molA��0.8molB���ﵽƽ��ʱ��A��ת���ʴ���50% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ҵ�г����ұ�����ķ����Ʊ�����ϩ��
������ҵ�г����ұ�����ķ����Ʊ�����ϩ�� ��g����
��g����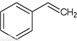 ��g��+H2��g������H=+117.6kJ/mol���٢ڵĻ�ѧ��Ӧƽ�ⳣ���ֱ�ΪK1��K2��
��g��+H2��g������H=+117.6kJ/mol���٢ڵĻ�ѧ��Ӧƽ�ⳣ���ֱ�ΪK1��K2�� ��g��+CO��g��+H2O��g�� ��H=+158.8 kJ/mol�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=K1•K2����K1��K2��ʾ��
��g��+CO��g��+H2O��g�� ��H=+158.8 kJ/mol�÷�Ӧ�Ļ�ѧƽ�ⳣ��K=K1•K2����K1��K2��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij���ȷ�Ӧ���Է����У���˸÷�Ӧ��������Ӧ | |
| B�� | 2NO��g��+2CO��g���TN2��g��+2CO2��g���ڳ��������Է����У���÷�Ӧ�ġ�H��0 | |
| C�� | ��ӦNH3��g��+HCl��g���TNH4Cl��s���������¿��Է����У���÷�Ӧ�ġ�H��0 | |
| D�� | CaCO3��s���TCaO��s��+CO2��g�������²����Է����У�˵���÷�Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com