
分析 Ⅰ.配离子中由中心离子提供空轨道、配体提供孤电子对;
Ⅱ.(1)氯化铁溶液发生水解,结合平衡移动原理分析解答;
(4)题目信息中,草酸铁能溶于水和酸,不溶于醇和醚,洗涤应尽可能减少样品损失;
Ⅲ.(2)实验Ⅱ中FeCl3与H2C2O4溶液反应生成Fe2(C2O4)3;可知氧化铁与草酸反应生成Fe2(C2O4)3与水;
(3)利用KSCN溶液检验溶液中铁离子,再加入草酸,若生成了[Fe(C2O4)3]3-配离子,溶液颜色变浅,然后对比颜色变化;
(4)应避免生成[Fe(C2O4)3]3-配离子,需要控制加入草酸的量.
解答 解:Ⅰ.Fe3+离子含有空轨道,C2O42-离子有孤电子对,故配体为:C2O42-,
故答案为:C2O42-;
Ⅱ.(1)由于氯化铁溶液发生水解,将氯化铁溶解在盐酸中,可以抑制FeCl3水解,
故答案为:抑制FeCl3水解;
(4)题目信息中,草酸铁能溶于水和酸,不溶于醇和醚,用酒精洗涤除去杂质、减少草酸铁因溶解损耗,
故答案为:除去杂质、减少草酸铁因溶解损耗;
Ⅲ.(2)实验Ⅱ中FeCl3与H2C2O4溶液反应生成Fe2(C2O4)3,不可能发生氧化还原反应,假设i是错误的;可知氧化铁与草酸反应生成Fe2(C2O4)3与水,反应方程式为:Fe2O3+3H2C2O4=Fe2(C2O4)3+3H2O,
故答案为:由于Fe2(C2O4)3存在,不可能发生氧化还原反应;Fe2O3+3H2C2O4=Fe2(C2O4)3+3H2O;
(3)利用KSCN溶液检验溶液中铁离子,再加入草酸,对比颜色变化,具体方案为:取少量草酸铁晶体溶于水,滴入几滴KSCN溶液,溶液变红,将溶液分到2支试管中,一支试管中再加入过量的草酸钾晶体,充分振荡,观察到红色明显比另一支浅很多,
故答案为:取少量草酸铁晶体溶于水,滴入几滴KSCN溶液,溶液变红,将溶液分到2支试管中,一支试管中再加入过量的草酸钾晶体,充分振荡,观察到红色明显比另一支浅很多;
(4)应避免生成[Fe(C2O4)3]3-配离子,需要控制加入草酸的量或控制氯化铁与草酸的比例,
故答案为:加入草酸的量(或氯化铁与草酸的比例).
点评 本题考查实验制备与探究,是对学生综合能力的考查,注意对题目信息的运用,难度中等,注意操作的规范性及实验现象、实验原理.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
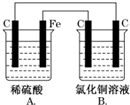 烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )
烧杯A中盛放0.1mol•L-1的H2SO4溶液,烧杯B中盛放0.1mol•L-1的CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )| A. | A烧杯中电解质溶液pH变大 | |
| B. | B烧杯中阳离子从左向右移动 | |
| C. | 当A烧杯中产生0.1 mol气体时,B烧杯中产生气体为0.1 mol | |
| D. | 一段时间后,B烧杯中溶液的浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Fe2+、NO3-、SO42- | B. | Na+、H+、AlO2-、HCO3- | ||
| C. | Ca2+、Fe3+、CO32-、CH3COO- | D. | Ca2+、Na+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | K+、Na+、NO3-、CO32-在碱性溶液中能大量共存 | |
| B. | Na+ K+ OH- Cl-在强酸性溶液中能大量共存 | |
| C. | Cu2+、H+、NO3-、SO42-能形成无色透明的溶液 | |
| D. | Ba2+、Na+、Cl-、SO42-在溶液中不能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠溶液中滴入硝酸银溶液 | B. | 金属钠在氯气中燃烧生成氯化钠 | ||
| C. | 铁片置于硫酸铜溶液中 | D. | 氢氧化钠溶液与稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②④ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色植物光合作用过程中是由太阳能转变成化学能 | |
| B. | 研制乙醇汽油技术,可降低机动车辆尾气中有害气体的排放 | |
| C. | 煤、石油、天然气属于可再生能源 | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com