
| A. | 氯化铁溶液与碘化钾溶液反应:Fe3++2I-═Fe2++I2 | |
| B. | 硫酸溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 氯化镁溶液与过量氨水反应:Mg2++2NH3•H2O═Mg (OH)2↓+2NH4+ |
分析 A.离子方程式两边总电荷不相等,违反了电荷守恒;
B.硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水;
C.醋酸为弱酸,离子方程式中醋酸不能拆开,需要保留分子式;
D.氯化镁溶液与氨水反应生成氢氧化铝沉淀和氯化铵.
解答 解:A.氯化铁溶液与碘化钾溶液反应生成氯化亚铁和碘单质,正确的离子方程式为:2Fe3++2I-═2Fe2++I2,故A错误;
B.硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故B错误;
C.醋酸溶液与CaCO3的反应中,碳酸钙和醋酸都需要保留化学式,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故C错误;
D.氯化镁溶液与过量氨水反应的离子方程式为:Mg2++2NH3•H2O═Mg (OH)2↓+2NH4+,故D正确;
故选D.
点评 本题考查了离子方程式书写方法,为高考的高频题,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
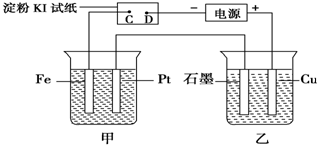
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+ | B. | Al3+ | C. | CH3COO- | D. | HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
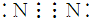 .
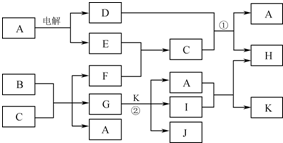
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素、蛋白质、油脂都是天然有机高分子化合物 | |
| B. | 燃煤中加入CaO后可减少酸雨的发生气体的排放 | |
| C. | 纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一 | |
| D. | 明矾是一种水处理剂,可用于水的杀菌、消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 23gNa变为Na+时失去的电子数为NA | B. | 18g水的电子数为NA | ||
| C. | 8gHe所含的分子数为NA | D. | 16gO2与16gO3所含的原子数均为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com