


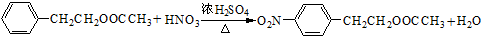
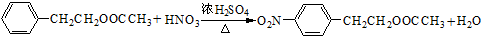
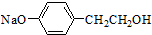
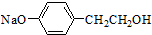
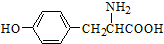
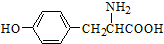

 ,所以C的结构简式为:
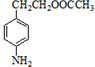
,所以C的结构简式为: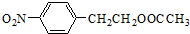 ,B和浓硝酸发生取代反应生成C,所以B的结构简式为:
,B和浓硝酸发生取代反应生成C,所以B的结构简式为: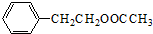 ,A和羧酸生成酯B,所以A的结构简式为:
,A和羧酸生成酯B,所以A的结构简式为: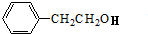 ,
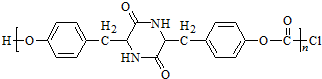
, 和氢氧化钠溶液发生水解反应生成D,化合物D苯环上的一氯代物有2种,结合D的分子式知,D的结构简式为
和氢氧化钠溶液发生水解反应生成D,化合物D苯环上的一氯代物有2种,结合D的分子式知,D的结构简式为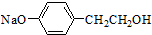 ,D反应生成E,结合E的分子式知,E的结构简式为:
,D反应生成E,结合E的分子式知,E的结构简式为: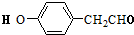 ,E发生一系列反应生成F,根据题给信息知,F的结构简式为:
,E发生一系列反应生成F,根据题给信息知,F的结构简式为: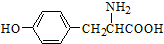 ,F发生反应生成G,G和
,F发生反应生成G,G和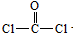 反应生成P,P的结构简式为:
反应生成P,P的结构简式为: .
. ,所以C的结构简式为:
,所以C的结构简式为: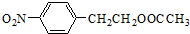 ,B和浓硝酸发生取代反应生成C,所以B的结构简式为:
,B和浓硝酸发生取代反应生成C,所以B的结构简式为: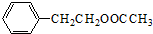 ,A和羧酸生成酯B,所以A的结构简式为:
,A和羧酸生成酯B,所以A的结构简式为: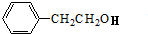 ,
, 和氢氧化钠溶液发生水解反应生成D,化合物D苯环上的一氯代物有2种,结合D的分子式知,D的结构简式为
和氢氧化钠溶液发生水解反应生成D,化合物D苯环上的一氯代物有2种,结合D的分子式知,D的结构简式为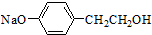 ,D反应生成E,结合E的分子式知,E的结构简式为:
,D反应生成E,结合E的分子式知,E的结构简式为: ,E发生一系列反应生成F,根据题给信息知,F的结构简式为:
,E发生一系列反应生成F,根据题给信息知,F的结构简式为: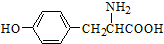 ,F发生反应生成G,G和
,F发生反应生成G,G和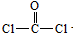 反应生成P,P的结构简式为:
反应生成P,P的结构简式为: .
.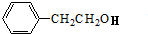 ,所以A中含有的官能团是醇羟基,故答案为:醇羟基;
,所以A中含有的官能团是醇羟基,故答案为:醇羟基;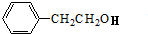 ,B的结构简式为:
,B的结构简式为: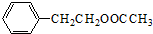 ,根据AB的结构简式知,该羧酸是乙酸,乙酸是弱电解质,乙酸中存在电离平衡,所以乙酸的电离方程式为:CH3COOH?CH3COO-+H+,故答案为:CH3COOH?CH3COO-+H+;
,根据AB的结构简式知,该羧酸是乙酸,乙酸是弱电解质,乙酸中存在电离平衡,所以乙酸的电离方程式为:CH3COOH?CH3COO-+H+,故答案为:CH3COOH?CH3COO-+H+;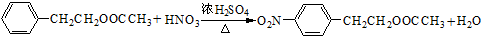 ,
,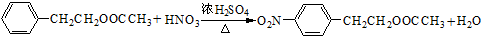 ;
;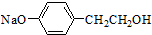 ,故答案为:
,故答案为: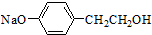 ;
;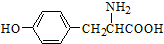 ,故答案为:
,故答案为: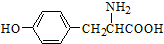 ;
; ,
, .
.

 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:

| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:

| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 操作 | 现象 |
| 取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
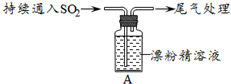 |
i.液面上方出现白雾; ⅱ.稍后,出现浑浊,溶液变为黄绿色; ⅲ.稍后,产生大量白色沉淀,黄绿色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com