
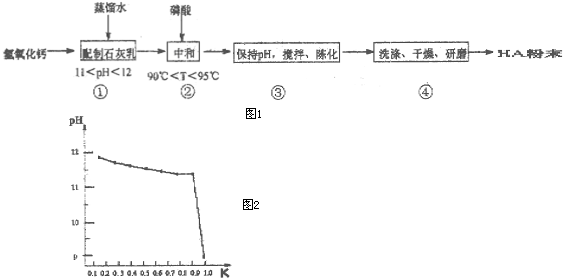
分析 (1)根据广泛pH试纸的使用方法答题;
(2)步骤②中温度控制在90℃~95℃,据此可确定适宜的加热方式;
(3)步骤②、③中都有固体参加反应,为使反应物质能充分接触而进行反应,必须充分搅拌;
(4)洗涤沉淀可以除去其中可溶性杂质;
(5)根据pH随“磷酸的用量与理论量比值”(用K表示)的变化如图2可知,在K为0.9至1.0之间,PH值变减小得非常快,此时需要严格控制滴定速率;
(6)根据元素守恒可写出氢氧化钙与磷酸中和生成HA的化学方程式.
解答 解:(1)用广泛pH试纸测溶液的pH值的方法为取一片pH试纸放在玻璃片(表面皿)上,用洁净干燥的玻璃棒蘸取待测液,滴在pH试纸上,把pH试纸显示的颜色半分钟内与标准比色卡对照,读出pH值,
故答案为:取一片pH试纸放在玻璃片(表面皿)上,用洁净干燥的玻璃棒蘸取待测液,滴在pH试纸上,把pH试纸显示的颜色半分钟内与标准比色卡对照,读出pH值;
(2)步骤②中温度控制在90℃~95℃,所以可以用水浴加热,
故答案为:水浴加热;
(3)步骤②、③中都有固体参加反应,充分搅拌可以使反应物质能充分接触而充分反应,保证产品的纯度,
故答案为:使反应物充分混合,保证产品的纯度;
(4)洗涤沉淀的目的是除去其中可溶性杂质,
故答案为:除去其中可溶性杂质;
(5)根据pH随“磷酸的用量与理论量比值”(用K表示)的变化如图2可知,在K为0.9至1.0之间,PH值变减小得非常快,此时需要严格控制滴定速率,
故答案为:0.9~1.0;
(6)根据元素守恒可知,氢氧化钙与磷酸中和生成HA的化学方程式为10Ca(OH)2+6H3PO4=Ca10(PO4)6(OH)2+18H2O,
故答案为:10Ca(OH)2+6H3PO4=Ca10(PO4)6(OH)2+18H2O.
点评 本题以羟基磷灰石的制备为载体,考查了工业流程分析、实验基础操作、图象分析等知识,难度不大,侧重考查学生运用基础知识分析问题、解决问题的能力.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 在硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产生,说明Ksp(BaCO3)<Ksp(BaSO4) | |
| B. | 测得Na2CO3溶液的pH大于同浓度的Na2SO3溶液,说明非金属性C<S | |
| C. | 用激光笔分别照射蛋清溶液和葡萄糖溶液,能产生光亮“通路”的是蛋清溶液 | |
| D. | 在淀粉溶液中加入稀硫酸并加热片刻再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶粒可以导电 | B. | 胶体是混合物 | ||
| C. | 胶体粒子大小在1~100nm之间 | D. | 胶体的分散剂为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50 mL 0.1 mol/L的NaCl溶液 | B. | 100 mL 0.2 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
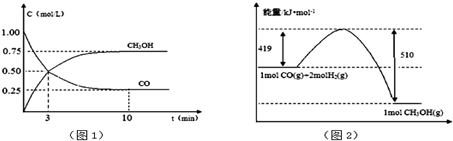
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硫酸工业生产过程在接触室中运用热交换技术可充分利用能源 | |
| B. | 联合制碱法生产纯碱时,先通入二氧化碳,再通入氨气 | |
| C. | 氯碱工业是以利用电解食盐水生产氯气、氢气和氢氧化钠为基础的工业体系 | |
| D. | 合成氨工业汇总,加入催化剂可提高氢气的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质参加的化合反应和有单质生成的分解反应属于氧化还原反应 | |
| B. | 没有单质参加的化合反应和没有单质生成的分解反应不属于氧化还原反应 | |
| C. | 复分解反应完全属于非氧化还原反应 | |
| D. | 置换反应完全属于氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com