
| A. | 亚硝酸钠具有氧化性,不可能表现出还原性 | |
| B. | 该反应中氧化剂与还原剂的物质的量之比为1:1 | |
| C. | 向反应所得的混合溶液中加入稀硫酸和亚硝酸钠,I-不可能转化为I2 | |
| D. | 人误食亚硝酸钠中毒时,可服用氢碘酸解毒 |
分析 由反应4HI+2NaNO2═2NaI+I2+2NO↑+2H2O,NaNO2 →NO,N元素的化合价+3价→+2价,得电子,所以NaNO2是氧化剂,HI→I2,碘元素化合价-1价→0价,失电子,所以HI是还原剂,据此分析解答.
A.根据化合价的变化判断氧化性和还原性;
B.根据HI一半是作酸、一半作还原剂来计算;
C.根据NaNO2在酸性条件下可以将碘离子氧化成碘单质判断;
D.根据反应产物NO有毒.
解答 解:A.由反应4HI+2NaNO2═2NaI+I2+2NO↑+2H2O,NaNO2 →NO,N元素的化合价+3价→+2价,所以NaNO2具有氧化性,但N元素的化合价+3价还可以升高,则还可能表现出还原性,故A错误;
B.该反应中氧化剂为NaNO2,4HI参与反应,只有2HI→I2,碘元素化合价-1价→0价,失电子,所以2HI是还原剂,所以氧化剂与还原剂的物质的量之比为2:2=1:1,故B正确;
C.由反应4HI+2NaNO2═2NaI+I2+2NO↑+2H2O可知,NaNO2在酸性条件下可以将碘离子氧化成碘单质,所以向反应所得的混合溶液中加入稀硫酸和亚硝酸钠,I-被氧化成I2,故C错误;
D.人误食亚硝酸钠中毒时,服用HI溶液产生有毒的NO,故D错误;
故选B.
点评 本题考查了有关氧化还原反应的知识,正确分析HI的作用是解题的关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 通过盐析作用析出的蛋白质固体不溶于水 | |
| B. | 淀粉、纤维素和葡萄糖均可发生水解 | |
| C. | 油脂在酸性条件下的水解反应叫做皂化反应 | |
| D. | 紫外线可使蛋白质变性,可利用紫外线进行消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1molNaCl固体中含0.1NA个阳离子 | |
| B. | 22.4LCO2含有的原子数是3NA | |
| C. | 常温常压下,NA个H2质量为2g | |
| D. | 1molMg与足量O2反应,失去的电子数是2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 可逆反应 FeCl3(aq)+3KSCN(aq)═Fe(SCN)3(aq)+3KCl(aq) 建立平衡后,在其它条件不变时,加入KC1固体,观察体系颜色的变化. | 验证浓度对化学平衡 的影响 |
| B | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和硫酸中,观察气泡产生的快慢. | 验证固体接触面积对 化学反应速率的影响 |
| C | 相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量MnO2固体. | 验证不同催化剂对 H2O2分解速率的影响 |
| D | 将S02气体通入溴水中,观察溶液颜色的变化 | 证明S02具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
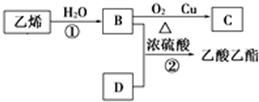
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com