
| A. | 各元素对应的离子半径顺序为:R>W>Z>Y | |
| B. | 气态氢化物的稳定性及还原性:HmW>HnR | |
| C. | XYR、X2W6、R2W2分子中所有原子均满足8电子结构 | |
| D. | 某气体通入品红溶液,溶液颜色褪去,则该气体一定是RY2 |
分析 X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成Z2Y2、Z2Y类型的化合物,则Z为Na、Y为O,其中Y、R同主族,它们可组成RY3化合物可知R为S;Z、R、W同周期,W为第三周期元素,结合组成XW4化合物可知,X为C,W为Cl,以此来解答.
解答 解:X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成Z2Y2、Z2Y类型的化合物,则Z为Na、Y为O,其中Y、R同主族,它们可组成RY3化合物可知R为S;Z、R、W同周期,W为第三周期元素,结合组成XW4化合物可知,X为C,W为Cl,
A.电子层越多,离子半径越大,具有相同排布的离子原子序数大的离子半径小,则离子半径为R>W>Y>Z,故A错误;
B.非金属性越强,氢化物越稳定,对应氢化物还原性越弱,则气态氢化物的稳定性为HmW>HnR,气态氢化物的还原性为HmW<HnR,故B错误;
C.XYR、X2W6、R2W2分子分别为COS、C2Cl6、S2Cl2,分子中所有原子均满足8电子结构,故C正确;
D.某气体通入品红溶液,溶液颜色褪去,气体可能为氯气、二氧化硫等,故D错误;
故选C.
点评 本题考查原子结构与元素周期律的关系,为高频考点,把握短周期及常见化合物的组成推断元素为解答的关键,侧重分析与推断能力的综合考查,充分考查了学生灵活应用基础知识的能力,注意规律性知识的应用,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学反应一定只伴随热量的变化 | |
| B. | 凡是吸热或放热过程中热量的变化均称为反应热 | |
| C. | 若△H<0,则反应物的能量高于生成物的能量 | |
| D. | 若△H>0,则反应物的能量高于生成物的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用铁作电极电解饱和氯化钠溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 高锰酸钾在酸性介质中与草酸反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8 H2O | |
| C. | FeCl2与K3[Fe(CN)6]反应:2Fe2++3[Fe(CN)6]3-═Fe2[Fe(CN)6]3↓ | |
| D. | 向KI和H2SO4的混合溶液中通入空气:4H++4I-+O2=2I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 g | B. | 2.4 g | C. | 3.2 g | D. | 4.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50 mL | B. | 100 mL | C. | 200 mL | D. | 300 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
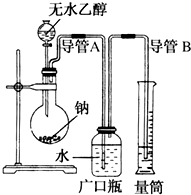 为了确定乙醇分子的结构简式是CH3-O-CH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子数目.试回答下列问题:
为了确定乙醇分子的结构简式是CH3-O-CH3还是CH3CH2OH,实验室利用右图所示的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子数目.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Al3+、Mg2+、SO32- | B. | K+、CO32-、I- | C. | Al3+、CO32-、I- | D. | Na+、Br-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
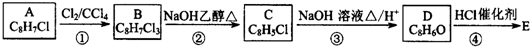
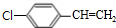 ,B中含有的官能团是氯原子.
,B中含有的官能团是氯原子.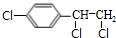 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$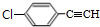 +2NaCl+2H2O,其反应类型为消去反应.
+2NaCl+2H2O,其反应类型为消去反应.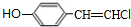 ;
;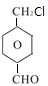 、
、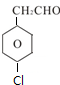 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L N2和O2混合气体中所含分子数为0.5NA | |
| B. | 6g SiO2所含分子数为0.1NA,化学键总数为0.4NA | |
| C. | 常温常压下,20g ND3中所含质子数为10NA | |
| D. | 向含0.2mol NH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀完全溶解,消耗的OH-数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com