
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
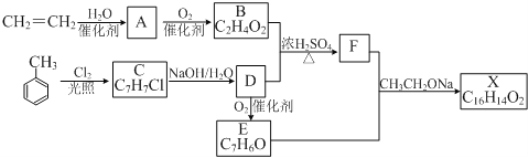
已知:![]() 。请回答:
。请回答:
(1)E中含氧官能团的名称是__________________。
(2)B+D→F的化学方程式____________,除F外图中与该反应类型相同的反应生成了_________(填A—F或X)。
(3)X的结构简式________关于化合物X,下列说法正确的是_______
A.能发生水解反应 B.不与浓硝酸发生取代反应
C.遇溴水会发生取代反应 D.能发生银镜反应
(4)写出一种同时符合下列条件的F的同分异构体,其结构简式为___________
ⅰ. 能发生银镜反应; ⅱ. 能使FeCl3(aq)显色;ⅲ. 有4中不同化学环境的氢原子
(5)乙烯是一种重要的化工原料。若在实验室想通过乙烯制备少量聚氯乙烯,写出可行的合成路线_________(其他无机原料任选)(合成路线的常用表示方法为:![]() 目标产物)
目标产物)
【答案】醛基 CH3COOH+![]()
![]()
![]() +H2O CDX
+H2O CDX ![]() A :
A :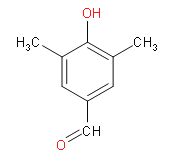 或
或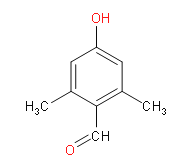 CH2=CH2
CH2=CH2![]() CH2Br-CH2Br
CH2Br-CH2Br![]() CH
CH![]() CH
CH![]() CH2=CHCl
CH2=CHCl![]()
![]()
【解析】
乙烯与水在催化剂作用下发生加成反应生成A是CH3CH2OH,乙醇催化氧化最终生成B是CH3COOH,甲苯转化得到D,D发生催化氧化得到E(C7H6O),则D为![]() ,E为
,E为![]() ,故甲苯在光照条件下与氯气发生的是取代反应生成C为
,故甲苯在光照条件下与氯气发生的是取代反应生成C为![]() ,然后在氢氧化钠的水溶液、加热条件下发生取代反应生成
,然后在氢氧化钠的水溶液、加热条件下发生取代反应生成![]() .乙酸与苯甲醇发生酯化反应生成F为
.乙酸与苯甲醇发生酯化反应生成F为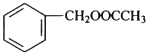 ,由信息可知F与苯甲醛反应生成X为
,由信息可知F与苯甲醛反应生成X为![]() 。
。
(1)E为![]() ,含有的官能团为:醛基,故答案为:醛基;
,含有的官能团为:醛基,故答案为:醛基;
(2)B+D→F的化学方程式:![]() ,该反应为取代反应,另外取代反应还生成了CDX,故答案为:
,该反应为取代反应,另外取代反应还生成了CDX,故答案为:![]() ;CDX;
;CDX;
(3)X的结构简式为![]() ,则:
,则:
A、X中含有酯基,能发生水解反应,故A正确;
B、X中含有苯环,能与浓硝酸发生取代反应,故B
C、X中含有碳碳双键,能使Br2水褪色,发生加成反应,故C错误;
D、X中不含有醛基,不能发生银镜反应,故D错误。
故答案为:![]() ;A;
;A;
(4)F为![]() ,其同分异构需满足下列条件:ⅰ. 能发生银镜反应:说明含有醛基;ⅱ. 能使FeCl3(aq)显色:说明有酚羟基;ⅲ. 有4中不同化学环境的氢原子:有4种等效氢,结构对称;根据上述分析,满足上述条件的结构为
,其同分异构需满足下列条件:ⅰ. 能发生银镜反应:说明含有醛基;ⅱ. 能使FeCl3(aq)显色:说明有酚羟基;ⅲ. 有4中不同化学环境的氢原子:有4种等效氢,结构对称;根据上述分析,满足上述条件的结构为 或
或 ;故答案为:
;故答案为: 或
或 ;
;
(5)实验室中通过乙烯制备少量聚氯乙烯,乙烯先通过加成反应生成1,2-二溴乙烷,再消去得到乙炔,乙炔再与HCl加成,最后再加聚,合成路线:CH2=CH2![]() CH2Br-CH2Br
CH2Br-CH2Br![]() CH
CH![]() CH
CH![]() CH2=CHCl
CH2=CHCl![]()
![]() ;故答案为:CH2=CH2
;故答案为:CH2=CH2![]() CH2Br-CH2Br
CH2Br-CH2Br![]() CH
CH![]() CH
CH![]() CH2=CHCl
CH2=CHCl![]()
![]() 。
。


科目:高中化学 来源: 题型:
【题目】实验室常利用“棕色环”现象检验NO3— 离子。其方法为:取含有 NO3— 的溶液于试管中,加入 FeSO4 溶液振荡,然后沿着试管内壁加入浓 H2SO4,在溶液的界面上岀现“棕色环”。回答下列问题:
(1)基态 Fe2+核外未成对电子个数为_____。
(2)形成“棕色环”主要发生如下反应:
3[Fe( H2O)6]2+ + NO3-+4H+ =3[Fe(H2O)6]3+ + NO ↑+2H2O
[Fe( H2O)6]2+ + NO=[Fe(NO) (H2O)5]2+(棕色)+ H2O
[Fe(NO)(H2O)5]2+中,配体是______、______,配位数为______。
(3)与 NO 互为等电子体的微粒是_____ (任写一例)。
(4)SO42-的空间构型是_____,其中 S 原子的杂化方式是________ 。
(5)铁原子在不同温度下排列构成不同晶体结构,在 912℃以下排列构成的晶体叫做α-铁; 在 912℃至 1394℃之间排列构成的晶体叫做γ -铁;在 1394℃以上排列构成的晶体, 叫做δ-铁。晶胞剖面结构如图所示:
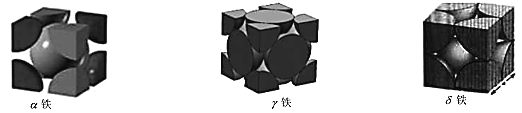
①α-铁的原子堆积方式为 _____ 。δ-铁配位数为 ____ 。
②已知γ-铁晶体密度为d g/cm3,则 Fe 原子的半径为____nm(用含 d、NA 的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】诺贝尔奖获得者屠呦呦带领团队发现了青蒿素,为中医药科技创新和人类健康事业作出巨大贡献。我国化学家在确认青蒿素分子结构之后实现了青蒿素的全合成。根据信息(部分条件和步骤已省略)回答下列问题:
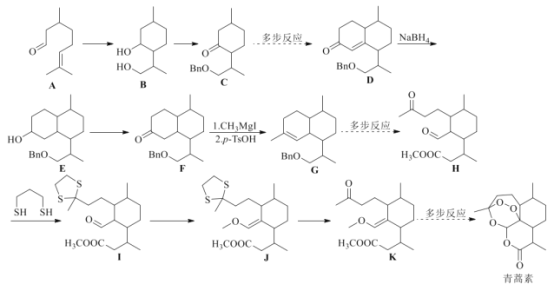
已知:![]() ,按要求回答下列问题:
,按要求回答下列问题:
(1)B的分子式为________________,所含官能团名称为________________________。![]() 的反应类型为________________。
的反应类型为________________。
(2)A的同系物中含碳原子数目最少的物质的结构简式为________________。A的同分异构体X含有醛基和六元碳环,且环上只有一个支链,满足上述条件的X有________种,其中核磁共振氢谱峰数最少的物质的结构简式为________________。
(3)写出A与银氨溶液反应的化学方程式________________________________。
(4)通过![]() 的反应,分子中引入了硫醚基团,而
的反应,分子中引入了硫醚基团,而![]()
![]() 的反应,分子中硫醚基团又被脱去,这样做的目的是________________。
的反应,分子中硫醚基团又被脱去,这样做的目的是________________。
(5)根据青蒿素所含官能团,推测其可能具有的性质________。
a.具有氧化性 b.可发生水解反应 c.易溶于水
(6)参照上述合成路线,写出以![]() 为主要原料,经四步反应制备
为主要原料,经四步反应制备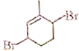 的流程。_____________
的流程。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是温度和压强对X+3Y![]() 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是
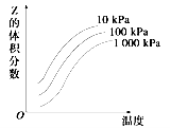
A.上述反应的正反应ΔH>0
B.升高温度,化学平衡常数K减小
C.X、Y、Z均为气态
D.当Y的浓度不再发生变化时,该反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫在自然界中以游离态和多种化合态形式出现,硫的化合物大多具有氧化性或还原性,许多金属硫化物难溶于水。完成下列填空:
(1)SO2能使KMnO4溶液褪色,还原产物是MnSO4,写出该反应的化学方程式__________。
(2)将SO2通入BaCl2溶液至饱和,未见沉淀生成,滴加溴水后,出现白色沉淀,该白色沉淀化学式为________。
(3)向Na2S固体中分别加入浓硫酸和稀硫酸,所得产物__________(填“相同”或“不同”),由此可知硫酸氧化性的强弱与__________有关。
(4)已知NaHSO3溶液显酸性,溶液中离子浓度由大到小的顺序是_____________。
(5)为了使Na2S溶液中c(Na+)/c(S2)的比值变小,可适量加入(或通入)的物质是___________
a.H2S气体 b.NaOH固体 c.HCl气体 d.KOH固体
(6)在图中,从A管通入一定量SO2后,在B处检测到有新的气体生成。B处排出的气体中(填“含”或“不含”)___________H2S。(已知:酸性H2SO4>H2CO3≈H2S)
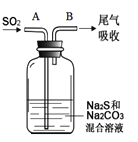
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中充入1mol N2和3molH2,一定条件下发生反应N2(g) + 3H2(g) ![]() 2NH3(g),达到化学平衡时,下列说法正确的是( )
2NH3(g),达到化学平衡时,下列说法正确的是( )
A.反应停止了B.正逆反应速率相等
C.N2的浓度为0D.H2的转化率为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置或操作能达到实验目的的是
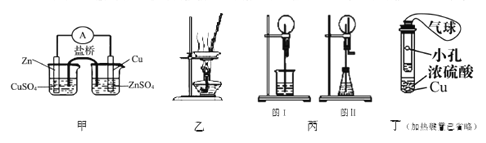
A. 甲装置构成铜锌原电池
B. 用图乙所示装量加热AlCl3饱和溶液然后利用余热蒸干制备AlCl3固体
C. 丙装置里图I烧瓶中充满氨气,烧杯中盛装水,在图II的锥形瓶中,加入足量的Cu与稀硝酸,图I和图II都产生喷泉现象且原理相同
D. 利用丁装置制取SO2,并检验其还原性,小试管中的试剂可为酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应叙述相符的是
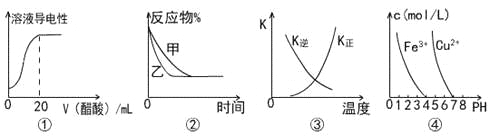
A.图①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液导电性随加入酸体积的变化
B.图②表示压强对可逆反应A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图③中曲线表示反应3A(g) + B(g)![]() 2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
2C(g)△H<0,正、逆反应的平衡常数K随温度的变化
D.据图④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以CaO和HNO3为原料制备Ca(NO3)26H2O晶体。为确保制备过程中既不补充水分,也无多余的水分,所用硝酸溶液中溶质的质量分数应为
A.53.8%B.58.3%C.60.3%D.70.0%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com