
分析 反应物浓度、温度、催化剂都影响化学反应速率,但决定物质反应速率的是物质本身的性质,外界条件只是影响因素,据此分析解答.
解答 解:(1)该反应中二氧化锰作催化剂,降低活化能,增大活化分子百分数,所以该反应中加入二氧化锰能加快化学反应速率,故答案为:催化剂;
(2)同浓度、同体积的盐酸中放入大小相同的铁片和镁片产生气体有快有慢是因为二者活泼性不同,即物质本身的性质,故答案为:物质的性质;
(3)盐酸的浓度不同导致其反应速率不同,盐酸浓度越大,其反应速率越大,故答案为:溶液的浓度;
(4)夏天温度高于冬天,温度越高化学反应速率越大,所以夏天的食品易霉变,冬天就不易发生类似现象,故答案为:温度.
点评 本题考查化学反应速率影响因素,为高频考点,明确温度、浓度、压强、催化剂等因素影响化学反应速率,但决定化学反应速率的是物质本身的性质,题目难度不大.


科目:高中化学 来源: 题型:实验题
 烟气的主要污染物是SO2、NOx,经臭氧预处理后再用适当溶液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
烟气的主要污染物是SO2、NOx,经臭氧预处理后再用适当溶液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
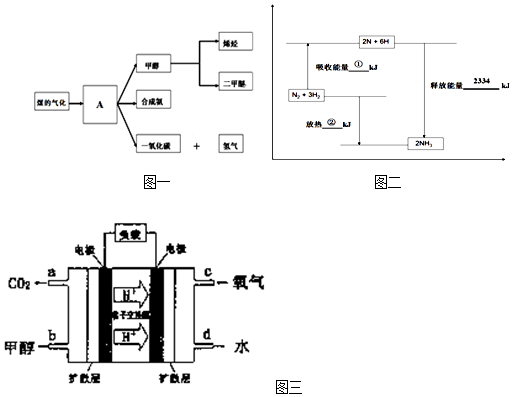
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- | |
| B. | 向AgCl沉淀中滴入稀KI溶液白色沉淀变黄,说明AgI比AgCl更难溶 | |
| C. | 先加入盐酸无沉淀,再加入BaCl2溶液产生白色沉淀,则试样中一定有SO42- | |
| D. | 盐溶液中加入NaOH微热,产生使湿润的红色石蕊试纸变蓝的气体,则一定是铵盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ③④⑤ | C. | 除④以外 | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b=c | B. | a>b>c | C. | a>c>b | D. | c>a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(NaOH)=0时,c(H+)=1×10-2mol•L-1 | |
| B. | V(NaOH)=10mL时,c(H+)=1×10-7mol•L-1 | |
| C. | V(NaOH)>10mL时,c(Na+)>c(C2O42-)>c(HC2O4-) | |
| D. | V(NaOH)<10mL时,不可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
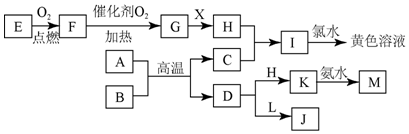
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com