
���ô�������Ӧ��![]() ת��Ϊ
ת��Ϊ![]() �ǹ�ҵ����������Ĺؼ����衣
�ǹ�ҵ����������Ĺؼ����衣
������֪��![]()
![]() ����
����![]() ��
��
�� (1)��![]() �¶�ʱ���÷�Ӧ��ƽ�ⳣ��
�¶�ʱ���÷�Ӧ��ƽ�ⳣ��![]() �����ڴ��¶��£���
�����ڴ��¶��£���![]() �ĺ����ܱ������У�����
�ĺ����ܱ������У�����![]() ��
��![]() ����Ӧ��ʼʱ����Ӧ�������� �淴Ӧ����(���������������=��)��
����Ӧ��ʼʱ����Ӧ�������� �淴Ӧ����(���������������=��)��
�� (2)��![]() �¶�ʱ����ʼ��
�¶�ʱ����ʼ��![]() ���ܱ������м���
���ܱ������м���![]() ��
��![]() ��һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����
��һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����![]() ����ʱ���������ת����Ϊ���� ��
����ʱ���������ת����Ϊ���� ��
(3)��(2)�еķ�Ӧ�ﵽƽ��ı�������������ʹ![]() ƽ��Ũ�ȱ�ԭ����С����
ƽ��Ũ�ȱ�ԭ����С����
�� ���� (����ĸ)��
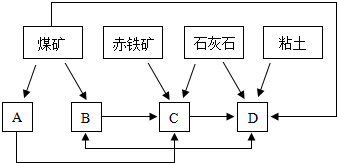
 A�������¶Ⱥ�����������䣬����
A�������¶Ⱥ�����������䣬����![]()
�� B�������¶Ⱥ�������ѹǿ���䣬����![]() ��
��![]()
�� C�������¶�
D����������������ʱ����С�������ݻ�
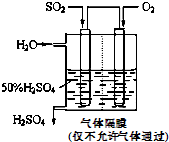
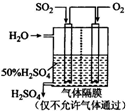
(4)������������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��
![]() �ĵ缫�ĵ缫��Ӧʽ���������������������������� ���� ��
�ĵ缫�ĵ缫��Ӧʽ���������������������������� ���� ��
(5)��������Ƶ������Ρ���һ���¶��£���![]() ��Һ�еμ�
��Һ�еμ�![]() ��Һ��
��Һ��![]() ��Һ�������ֳ�������ʱ��
��Һ�������ֳ�������ʱ��![]() �������������� ��[��֪���¶�ʱ��
�������������� ��[��֪���¶�ʱ��![]()
![]() ]
]

 �߲������Ӧ��һ��ͨϵ�д�
�߲������Ӧ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2011?������ģ�⣩���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮��֪��SO2��g��+
��2011?������ģ�⣩���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮��֪��SO2��g��+| 1 |
| 2 |
| 10 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
|
ѹǿ/MPa SO2ת���� �¶�/�� |
0.1 |
0.5 |
1 |
10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
| ||
| �� |
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| �� |
| ||
| �� |
| T/K | 303 | 313 | 323 |
| CA2������/��10-1mol�� | 4.3 | 5.9 | 6.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ѹǿ/Mpa ת����/% �¶�/�� |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ᱻ��Ϊ����ҵ֮ĸ����������ڹ�ҵ�����е���Ҫ��λ�����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ��������Ĺؼ����裮һ���¶��£���һ�������������Ϊ2L���ܱ������г���2.0mol SO2��g����1.0mol O2��g����������Ӧ��SO2��g��+
���ᱻ��Ϊ����ҵ֮ĸ����������ڹ�ҵ�����е���Ҫ��λ�����ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ��������Ĺؼ����裮һ���¶��£���һ�������������Ϊ2L���ܱ������г���2.0mol SO2��g����1.0mol O2��g����������Ӧ��SO2��g��+| 1 | 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com