
【题目】下列反应的离子方程式正确的是 ( )
A. 用醋酸除去水垢:2H++CaCO3===Ca2++CO2↑+H2O
B. 酸性氯化亚铁溶液中加入双氧水2Fe2++H2O2===2Fe3++O2↑+2H+
C. NaAlO2溶液中通入过量CO2:2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32-
D. 电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
【答案】D
【解析】
A.醋酸为弱酸,不能拆写;B.离子方程式两边正电荷不相等,Fe元素和O元素的化合价都升高;C.NaAlO2溶液中通入过量CO2生成HCO3-;D.电解饱和食盐水时,阳极上生成氯气、阴极上生成氢气同时阴极附近有NaOH生成。
用醋酸除去水垢反应的离子方程式为:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑,故A错误;酸性氯化亚铁溶液中加入双氧水,双氧水将亚铁离子氧化成铁离子,正确的离子方程式为:2Fe2++2H++H2O2═2Fe3++2H2O,B错误;Al(OH)3不溶于CO2,通入过量CO2生成HCO3-,反应的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,C错误;电解饱和食盐水时,阳极上生成氯气、阴极上生成氢气同时阴极附近有NaOH生成,离子方程式为2Cl-+2H2O![]() H2↑+Cl2↑+2OH-,D正确。
H2↑+Cl2↑+2OH-,D正确。
故选D。


科目:高中化学 来源: 题型:
【题目】铝土矿(主要成分为Al2O3,还含有杂质SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀 A、B的成分分别是____________、____________;步骤②中的试剂a是_________(以上均填化学式)。
(2)试写出步骤③中发生反应的离子方程式__________________。
(3)简述检验所得滤液甲中存在Fe3+的操作方法:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作与安全事故处理不正确的是( )
A.用试管夹从试管底部由下往上夹住距试管口约1/3处,手持试管夹长柄末端进行加热
B.将CO中毒者移动到通风处抢救
C.实验中剩余的钠不能再放回原试剂瓶
D.蒸馏烧瓶加热时需要垫石棉网
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需用480 mL 0.5 mol·L-1的NaOH溶液。
(1)该同学应选择________ mL的容量瓶。
(2)其操作步骤如下图所示,则如图操作应在下图中的__________(填选项字母)之间。

A.②与③ B.①与② C.④与⑤
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。

(4)下列操作对所配溶液的浓度偏大的有(填写下列序号)(_________)
①转移完溶液后未洗涤玻璃棒和烧杯 ②容量瓶中原来有少量蒸馏水
③摇匀后发现液面低于刻度线再加水 ④定容时观察液面俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2 L的密闭容器中,发生下列反应:3A(g)+B(g)xC(g)+2D(g),经2 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,以C表示的平均速率v(C)=0.25 mol·L-1·min-1,下列说法正确的是( )
A. 该反应方程式中,x=1 B. 2 min时,A的物质的量为0.75 mol
C. 2 min时,A的转化率为50% D. 反应速率v(B)=0.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 电子云图中的小黑点密表示该核外空间的电子多
B. 电子排布式 1s22s22px2违反了洪特规则
C. 原子序数为7、8、9的三种元素,其第一电离能和电负性均依次增大
D. 元素周期表中Fe处于ds区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型及分子结构示意图如下:

(1)下列有关石墨烯说法正确的是________。
A.石墨烯的结构与金刚石相似
B.石墨烯分子中所有原子可以处于同一平面
C.12 g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用力
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合。
①钴原子在基态时,核外电子排布式为________。
②乙醇沸点比氯乙烷高,主要原因是_______________________。
③下图是金与铜形成的金属互化物合金,它的化学式可表示为:________。
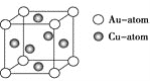
④含碳原子且属于非极性分子的是________;
a.甲烷 b.乙炔 c.苯 d.乙醇
⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:________。
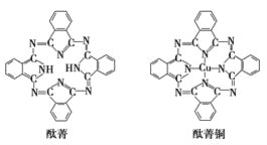
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图为几种晶体或晶胞的构型示意图。
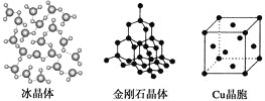

请回答下列问题:
(1)这些晶体中,粒子之间以共价键结合形成的晶体是_______________________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能________(填“大于”或“小于”)MgO晶体的晶格能,原因是___________________________________________。
(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰的重要原因是___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com