
【题目】浊液区别于其他分散系最本质的特征是( )
A.外观浑浊不清
B.浊液没有丁达尔现象
C.不稳定
D.分散质粒子直径大于100nm
 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】能用![]() +
+![]() → H2O表示的是
→ H2O表示的是
A. NaHSO4 + NaOH → Na2SO4 + H2O B. CH3COOH + NaOH → CH3COONa + H2O
C. H2SO4 + Ba(OH)2 → BaSO4↓ + 2H2O D. NH3 · H2O + HCl → NH4Cl + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸钠可以用于制备火箭推进剂高氯酸铵。以粗盐为原料制备高氯酸钠晶体(NaClO4·H2O)的流程如下:

(1)“精制”中,由粗盐(含Ca2+、Mg2+、SO42-等杂质)制备精制盐水时需用到NaOH、BaCl2、Na2CO3等试剂。加入Na2CO3溶液的作用
(2)“电解”分2步进行,其反应分别为NaCl+3H2O![]() NaClO3+3H2↑ NaClO3+H2O
NaClO3+3H2↑ NaClO3+H2O![]() NaClO4+H2↑
NaClO4+H2↑
(3)“除杂”的目的是除去少量未被电解的NaClO3,该反应的化学方程式为: ,
(4)“分离”的操作分别是加热浓缩、 、冷却结晶、过滤、洗涤、干燥。(各物质的溶解度如右图所示)
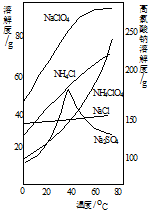
(5)室温下将得到的高氯酸钠晶体加入氯化铵饱和溶液中,反应的离子方程式为:
(6)为确定所得高氯酸钠晶体的纯度(含有少量Na2SO4杂质),进行如下实验:
①准确称取3.00 g样品加水充分溶解,所得溶液转移至容量瓶并配置成100 mL溶液。
②量取25.00 mL溶液,加入足量的KI溶液充分反应(ClO4-被还原成Cl-),再滴加1.000 mol·L-1 Na2S2O3溶液进行反应(反应为I2+2 Na2S2O3=2 NaI+ Na2S4O6),恰好消耗40.00 mL Na2S2O3溶液。
根据以上数据计算样品中高氯酸钠晶体纯度为: (写出计算过程,保留四位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.钠是一种强还原剂,可以将钛、铌等金属从其氯化物溶液中置换出来
B.铜能与氯化铁溶液反应,该反应可以应用于印刷电路板的制作
C.人们发现了118种元素,即共有118种核素
D.H2和D2互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为达到下列实验目的,所采用的方法合理的是( )
A.溴水中提取溴:分液
B.分离水和汽油的混合物:蒸馏
C.分离饱和食盐水和沙子的混合物:过滤
D.从硝酸钾和氯化钠混合液中获取硝酸钾:萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作错误的是( )
A.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.用酒精萃取碘水中的碘
D.配制浓H2SO4和浓HNO3的混酸时,应将H2SO4慢慢加到浓HNO3中,并及时搅拌和冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应中关于能量的比较正确的是( )
①H2(g)+Cl2(g)=2HCl(g)△H1; ![]() H2(g)+
H2(g)+![]() Cl2(g)=HCl (g)△H2;△H1>△H2
Cl2(g)=HCl (g)△H2;△H1>△H2
②2H2O(l)=2H2(g)+O2(g)△H1; 2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)△H2;△H1>△H2
③CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(l)△H1;CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H1;CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2
O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2
④t℃时,在一定条件下,将 1mol N2和 3mol H2 分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为 Q1、Q2; Q1<Q2.
A. ①③④ B. ①②④ C. ②③④ D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同一条件下,下列顺序关系不正确的是
A. 在水中的溶解度:乙二醇>溴乙烷
B. 溶液的pH:碳酸氢钠>苯酚钠
C. 沸点:CH3OH>HCHO
D. 与钠反应的快慢:水>乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得到分子式为C5H10的两种产物Y、Z。Y、Z经催化加氢后都可得到2甲基丁烷。则X的结构简式可能为( )
A. ![]() B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com