
【题目】钼(Mo)是一种难熔稀有金属,我国的钼储量居世界第二。钼及其合金在冶金,农业、电器、化工、环保等方面有着广泛的应用。
(1)已知:①2Mo(s)+3O2(g)=2MoO3(s) ΔH1
②MoS2(s) +2O2(g)=Mo(s)+2SO2(g) ΔH2
③2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g) ΔH3
则ΔH3=__________(用含ΔH1、ΔH2的代数式表示)。
(2)密闭容器中用Na2CO3(S)作固硫剂,同时用一定量氢气还原辉钼矿(MoS2)的原理是:MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s) +2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示:
Mo(s) +2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示:
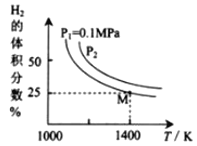
①由图可知,该反应的ΔH______0(填“>”或“<”);P2__________0.1MPa(填“>”或“<”)。
②如果上述反应在体积不变的密闭容器中达平衡,下列说法错误的是______(选填编号)。
A.v正(H2)=v逆(H2O)
B.再加入MoS2,则H2转化率增大
C.容器内气体的密度不变时,一定达平衡状态
D.容器内压强不变时,一定达平衡状态
③由图可知M点时氢气的平衡转化率为________(计算结果保留0.1%)。
④平衡常数可用平衡分压代替平衡浓度计算,气体分压=气体总压×物质的量分数。求图中M点的平衡常数Kp=______(MPa)2
【答案】△H1+2△H2 > > B 66.7% 0.01
【解析】
(1)根据盖斯定律进行计算;
(2)①温度越高,氢气含量越少,则说明反应为吸热反应;在相同温度下,P2条件下氢气含量大,说明此时反应向左进行;
②根据变量不变达平衡进行判断;
③依据三段式计算;
④根据平衡常数的含义计算。
(1)已知:①2Mo(s)+3O2(g)=2MoO3(s) ΔH1
②MoS2(s) +2O2(g)=Mo(s)+2SO2(g) ΔH2
根据盖斯定律,由方程式②×2+方程式①得到方程式③2MoS2(s)+7O2(g)=2MoO3(s)+4SO2(g),所以ΔH3=△H1+2△H2;
(2)①温度越高,氢气含量越少,则说明反应为吸热反应,反应体系能量升高,故ΔH>0;在相同温度下,P2条件下氢气含量大,说明此时反应向左进行,又方程式右端气体体积较左端大,增大压强会促进反应向左进行,则P2>P1=0.1MPa;
②A. 反应达到平衡时正逆反应速率相等,即v正(H2)=v逆(H2O),选项A正确;
B. 加入固体MoS2平衡不移动,氢气转化率不变,选项B错误;
C. 容器内气体的质量是变化的,而容器体积不变,因此容器内气体的密度不变时,一定达平衡状态,选项C正确;
D. 正反应是气体体积增大的可逆反应,因此容器内压强不变时,一定达平衡状态,选项D正确。
答案选B;
③设氢气的起始量是1mol,则根据方程式可知
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s) +2CO(g)+4H2O(g)+2Na2S(s)
Mo(s) +2CO(g)+4H2O(g)+2Na2S(s)
起始量(mol) 1 0 0
转化量(mol) x 0.5x x
平衡量(mol) 1-x 0.5x x
则![]()
解得x=2/3,则氢气的转化率为: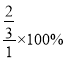 =66.7%;
=66.7%;
④根据③中分析可知平衡时各物质的量分数分别为:氢气:0.25,CO:0.25,水蒸气:0.5,所以Kp=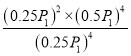 =P12=0.01 (MPa)2。
=P12=0.01 (MPa)2。


 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.盐酸滴入氨水中:H++OH-=H2O
B.碳酸氢根离子的水解:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
C.以石墨作电极电解氯化钾溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.硫酸铅蓄电池的正极反应为:PbO2+4H++2e-=Pb2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,将3molA和1molB两种气体混合于固定容积为2L密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(s)。2min末该反应达到平衡,生成0.6molD,并测得C的浓度为0.15mol/L。下列判断正确的是
xC(g)+2D(s)。2min末该反应达到平衡,生成0.6molD,并测得C的浓度为0.15mol/L。下列判断正确的是
A. 从开始到平衡A的平均反应速率为0.225mol/(Ls)
B. 从开始到平衡B的转化率为60%
C. 此反应的化学平衡常数表达式K=c(C)c2(D)/c3(A)c(B)
D. 若混合气体的密度不再改变时,该反应一定达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgCl2和AlCl3的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)关系如下图所示。
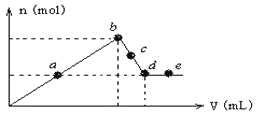
则下列说法正确的是( )
A.a、c两点沉淀物成份相同,d、e两点沉淀物成份相同
B.b—c段与c—d段溶液中阴离子的物质的量相等
C.在d点,向溶液中加入盐酸,沉淀量将减少
D.在反应过程中,各状态点溶液的pH大小顺序是:e > d > c > a > b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,错误的是( )
A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯
B.乙苯能发生氧化反应,但不能发生还原反应
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.苯乙烯在合适条件下催化加氢可生成乙基环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。
(2)如果按图中所示的装置进行试验,求得的中和热数值_______(填“偏大、偏小、无影响”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与(2)中实验相比,所求中和热_________ (填“相等”或“不相等”)。
Ⅱ: (1)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6),丙烷脱氢可得丙烯。已知:C3H8(g) === CH4(g)+HC≡CH(g)+H2(g) △H1=+156.6 kJ·mol-1
CH3CH=CH2(g)=== CH4(g)+ HC≡CH(g ) △H2=+32.4 kJ·mol-1
则C3H8(g) === CH3CH=CH2(g)+H2(g) △H =______________ kJ·mol-1。
(2)发射火箭时用肼(N2H4)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知32gN2H4(g)完全发生上述反应放出568kJ的热量,热化学方程式是:____________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大.金属W是制备手机电池的常用材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是它的电子层数的2倍。下列说法正确的是![]()
A.金属W具有两性
B.X、Z形成的化合物为离子化合物
C.Y与Z生成的化合物在水中会发生双水解
D.元素X与氢形成的原子个数比为1:1的化合物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. 氮原子的价电子排布图:![]()
B. 2p和3p轨道形状均为哑铃形,能量也相等
C. 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素
D. 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com