
| A. | 6体积 | B. | 4体积 | C. | 3体积 | D. | 无法确定 |
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
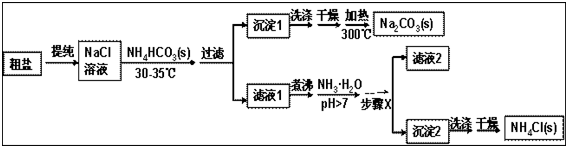
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g Fe与足量盐酸反应,反应中转移的电子数为0.3NA | |
| B. | 0.1 mol FeCl3完全水解转化为氢氧化铁胶体,生成0.1NA个胶粒 | |
| C. | 常温下,28 g的N2和CO混合气体含有的原子数为2NA | |
| D. | 1mol Na2O2和足量CO2充分反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+H2O═H2SO3 | B. | H2CO3═CO2↑+H2O | ||
| C. | 2NaOH+H2SO4═Na2SO4+2H2O | D. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体制备:向沸水中逐滴加入少量饱和硫酸铁溶液,继续加热煮沸至液体变为红褐色,停止加热 | |
| B. | 用容量瓶配制溶液时,定容时俯视刻度线,所配溶液浓度偏大 | |
| C. | 中和热实验,在操作时应将碱液分多次倒入酸中,以防液体溅出,产生误差 | |
| D. | 萃取碘水中的碘实验时,将碘水倒入分液漏斗,然后再注入乙醇,振荡、静置分层后,下层紫色液体先从下口放出,之后,上层无色液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L庚烷完全燃烧生成二氧化碳分子数为8NA | |
| B. | 28克由C3H6和C4H8组成的混合气体中含共用电子对数目为6NA个 | |
| C. | 0.1mol氧气作为氧化剂得到电子的数目一定为0.4NA | |
| D. | 常温下,0.1mol•L-1的碳酸钠溶液中含有的阴离子数大于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 向滤液a中加入适量溶液,可以得到白色沉淀 | |
| B. | 滤液b中加入氨水的目的是使沉淀,滤渣c为红褐色 | |
| C. | 要将Li从溶液中析出,可在滤液c中加入足量溶液,加热浓缩,冷却结晶 | |
| D. | 图中的氨水可以用适量NaOH溶液代替. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com