
| A.二氧化硅可用来制造现代通迅材料光导纤维 |
| B.N2是大气中的主要成分之一,雷雨时,可直接转化为NO2? |
| C.铜在潮湿的空气里很稳定不会被锈蚀 |
| D.硅是应用广泛的半导体材料,常温下只与氟气、氢氟酸反应不和任何其它物质反应 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
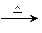 CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。试计算:
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。试计算:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
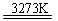 Si(粗)+2CO↑;SiO2+3C
Si(粗)+2CO↑;SiO2+3C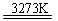 SiC+2CO↑。
SiC+2CO↑。 SiCl4(l); SiCl4+2H2
SiCl4(l); SiCl4+2H2 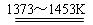 Si(纯)+4HCl。
Si(纯)+4HCl。 )和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂_______________吨。
)和SiCl4的利用率均为80%,制粗硅时有10%的SiO2转化为SiC,则生产25.2吨纯硅需纯度为75%石英砂_______________吨。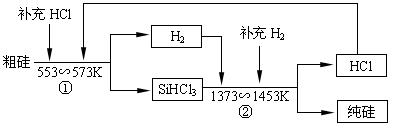
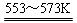 SiHCl3(l)+H2(g);
SiHCl3(l)+H2(g);查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硅是制备光导纤维的原料,光导纤维遇碱会“短路” |
| B.作半导体材料的硅位于周期表中金属与非金属分界线附近 |
| C.工业上,利用二氧化硅热分解法冶炼硅 |
| D.二氧化硅和硅属于同种晶体类型 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②⑤ | B.⑤④ | C.④② | D.④① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.SiO2+2C Si+2CO↑ Si+2CO↑ |
B.CaCO3+SiO2 CaSiO3+CO2↑ CaSiO3+CO2↑ |
| C.Na2SiO3+CO2+H20==Na2CO3+H2SiO4↓ |
D.Si+2 NaOH+H2O==Na2SiO3 NaOH+H2O==Na2SiO3 +2H2↑ +2H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com