
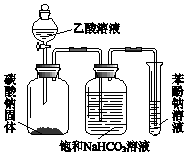
 某同学欲用如图所示装置比较苯酚、乙酸、碳酸的酸性强弱,实验进行一段时间后,盛有苯酚钠溶液的试管中溶液变浑浊.
某同学欲用如图所示装置比较苯酚、乙酸、碳酸的酸性强弱,实验进行一段时间后,盛有苯酚钠溶液的试管中溶液变浑浊.分析 比较苯酚、乙酸、碳酸的酸性,由实验装置可知,乙酸与碳酸钠发生CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O,饱和碳酸氢钠溶液除去挥发的乙酸,小试管中发生C6H5O-+CO2+H2O→C6H5OH+HCO3-,均为强酸制取弱酸的反应,可比较酸性,以此来解答.
解答 解:(1)苯酚钠溶液中发生反应的化学方程式是C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,故答案为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;
(2)饱和NaHCO3溶液的作用是除去二氧化碳中混有的乙酸,故答案为:除去二氧化碳中混有的乙酸;
(3)由CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O、C6H5O-+CO2+H2O→C6H5OH+HCO3-可知,均为强酸制取弱酸的反应,则苯酚、乙酸、碳酸的酸性由强到弱的顺序是乙酸>碳酸>苯酚,故答案为:乙酸>碳酸>苯酚.
点评 本题考查有机物酸性的比较,为高频考点,把握强酸制取弱酸的反应原理、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意乙酸易挥发,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成n mol A,同时生成n mol D | |
| B. | B的浓度保持不变 | |
| C. | 容器内混合气体的密度不随时间而变化 | |
| D. | 单位时间内消耗n mol B,同时消耗n mol A |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g甲烷含有的电子数为NA | |
| B. | 1L0.1mol•L-1NaHCO3溶液中含有的HCO3-数目为0.1NA | |
| C. | 1LpH=1的硫酸溶液中含有的H+数为0.2NA | |
| D. | 标准状况下,2.24LCO和CO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | Cl2通入FeCl2溶液中:Cl2+Fe2+═2Cl-+Fe3+ | |
| C. | 少量CO2通入澄清石灰水中:CO2+2OH-+Ca2+═Ca CO3↓+H2O | |
| D. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠的水解:HCO3-+H2O=H3+O+CO32- | |
| B. | 14g乙烯燃烧生成液态水产生b kJ热量,则表示其燃烧热的热化学方程式为:C2H4(g)+3O2(g)═2H2O(g)+2CO2(g)△H=-2b kJ•mol-1 | |
| C. | 用两根铜棒电解盐酸:2H++2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| D. | 在酸性碘化亚铁溶液中通入少量氧气:4I-+O2+4H+=2I2+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com