
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1
2H2(g)+O2(g)═2H2O(g)△H2
C(s)+O2(g)═CO2(g)△H3
则反应4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
|
| A. | 12△H3+5△H2﹣2△H1 | B. | 2△H1﹣5△H2﹣12△H3 | C. | 12△H3﹣5△H2﹣2△H1 | D. | △H1﹣5△H2﹣12△H3 |
| 有关反应热的计算;热化学方程式.. | |
| 专题: | 化学反应中的能量变化. |
| 分析: | 根据盖斯定律,利用方程式的加减得出C3H5(ONO2)3分解成CO2、N2、H2O、O2的化学方程式,其反应热也要相应的加减,从而得出其热化学反应方程式. |
| 解答: | 解:已知: ①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l)△H1 ②2H2(g)+O2(g)═2H2O(g)△H2 ③C(s)+O2(g)═CO2(g)△H3 由盖斯定律:5×②+12×③﹣2×①得:4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g)△H=12△H3+5△H2﹣2△H1; 故选A. |
| 点评: | 本题考查了反应热的计算,侧重于盖斯定律应用的考查,题目难度不大,准确把握盖斯定律的概念是关键. |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
阅读下列材料后回答问题:一个体重50Kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在。正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收。
(1)在人体中进行Fe2+ 的转化时,实现①的转化需消耗 剂(填氧化或还原),

Fe3+
通常用 (填试剂名称)检验Fe3+存在。
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作 剂,Fe3+发生 反应。
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的离子方程式为
。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+Cl2(g)  COCl2(g) ΔH<0,当反应达到平衡时,下列措施中能提高Cl2转化率的是
COCl2(g) ΔH<0,当反应达到平衡时,下列措施中能提高Cl2转化率的是
①升温 ②降温 ③增加CO浓度 ④加压 ⑤加催化剂 ⑥恒压通入惰性气体
A.①②④ B.①④⑥ C.②③④ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池是燃料(如CO、H2、CH4等)跟O2(或空气)反应,将化学能转化为电能的装置,电解质溶液是强碱溶液.下列关于CH4燃料电池的说法正确的是( )
|
| A. | 放电时溶液中的阴离子向正极移动 |
|
| B. | 负极反应式为:CH4+10OH﹣﹣8e﹣=CO32﹣+7H2O |
|
| C. | 随着放电的进行,溶液的pH不变 |
|
| D. | 负极反应式为:O2+2H2O+4e=4OH﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,对固定容器中的可逆反应A(g)+2B(g)⇌3C(g)的下列叙述中,能说明反应已达到平衡的是( )(A、B为无色气体,C为有色气体)
|
| A. | 混合气体的物质的量不再变化 |
|
| B. | 单位时间内消耗amolA,同时生成3amolC |
|
| C. | 容器内的压强不再变化 |
|
| D. | 容器内气体颜色不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(气)+B(气)xC(气)+2D(气),2分钟末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于 2 ;
(2)B的平衡浓度为 0.8mol/L ;
(3)A的转化率为 60% ;
(4)生成D的反应速率为 0.2mol/(L•min) .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某同学对相应的离子方程式所作的评价,其中评价合理的是
| 编号 | 化学反应 | 离子方程式 | 评 价 |
| A | 碳酸钙与醋酸 反应 | CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| B | NaAlO2溶液中通入过量CO2 | 2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32- | 正确 |
| C | NaHCO3的水解 | HCO3-+H2O ═ CO32-+H3O+ | 错误,水解方程式误写成电离方程式 |
| D | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①经分析某物质只含有一种元素,则该物质一定是单质;
②根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等;
③NO2和水反应能生成硝酸,但NO2不是酸性氧化物
④溶液是电中性的,胶体是带电的
⑤不能发生丁达尔效应的分散系有氯化钠溶液、水等
A.①③④ B.仅③ C.仅⑤ D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式_______________________。
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中,P元素的化合价为__________。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为___________(填化学式)。
③NaH2PO2为___________(填 “正盐”或“酸式盐”),其溶液显_______(填“弱酸性”、“中性”或“弱碱性”)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式_____
______________________________________。
(4)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
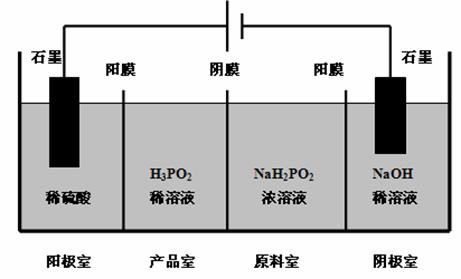
①写出阳极的电极反应____________________________________。
②分析产品室可得到H3PO2的原因___________________________________。
③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有 杂质,该杂质产生的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com