
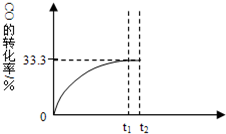
 ijĪĀ¶ČĻĀ£¬ĻņĆܱÕČŻĘ÷ÖŠ³äČė2.0mol COŗĶ1.0mol H2O£¬·¢Éś·“Ó¦£ŗ
ijĪĀ¶ČĻĀ£¬ĻņĆܱÕČŻĘ÷ÖŠ³äČė2.0mol COŗĶ1.0mol H2O£¬·¢Éś·“Ó¦£ŗ| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| (2/3V)2 |
| (4/3V)?(1/3V) |
| 2a?2a |
| (2-2a)?(2-2a) |
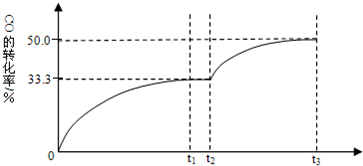 £¬
£¬ £®
£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢“Óŗ£“ųÖŠĢįČ”µāµ„ÖŹµÄ¹ż³Ģ²»Éę¼°Ńõ»Æ»¹Ō·“Ó¦ |
| B”¢ĶłµĖ®ÖŠ¼ÓČėNaClµČÅä³ÉČĖŌģŗ£Ė®£¬æÉÓĆÓŚŗ£²śĘ·µÄ³¤Ķ¾ŌĖŹä |
| C”¢³ą³±Ö÷ŅŖŹĒÓɹ¤Å©ŅµÉś²śŗĶÉś»ī·ĻĖ®ŅżĘšŃŲŗ£Ė®ÓņµÄø»ÓŖŃų»Æ¶ųŌģ³ÉµÄ |
| D”¢ĖäČ»ŗ£Ė®ÖŠŌŖĖŲµÄÖÖĄąŗܶą£¬×Ü“¢Įæŗܓ󣬵«Šķ¶ąŌŖĖŲµÄø»¼Æ³Ģ¶ČŗܵĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 1 |
| 2 |
| 1 |
| 4 |
| 3 |
| 4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢µČĪļÖŹµÄĮæµÄČõĖįHAÓėĘä¼ŲŃĪKAµÄ»ģŗĻČÜŅŗÖŠ£ŗ2c£ØK+£©=c£ØHA£©+c£ØA-£© |
| B”¢pHĻąĶ¬µÄCH3COONaČÜŅŗ”¢Ba£ØOH£©2ČÜŅŗ”¢KHCO3ČÜŅŗ£ŗc£ØK+£©£¾c£ØNa+£©£¾c£ØBa2+£© |
| C”¢°±Ė®ÖŠÖšµĪ¼ÓČėŃĪĖįµĆµ½µÄĖįŠŌČÜŅŗ£ŗc£ØCl-£©£¾c£ØNH4+£©£¾c£ØH+£©£¾c£ØOH-£© |
| D”¢pH=3µÄŅ»ŌŖĖįHAČÜŅŗŗĶpH=11µÄŅ»ŌŖ¼īMOHČÜŅŗµČĢå»ż»ģŗĻ£ŗc£ØM+£©=c£ØA-£©£¾c£ØH+£©=c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ČżĀČ»ÆĢśČÜŅŗÖŠ¼ÓČėĢś·ŪFe3++FeØT2Fe2+ |
B”¢¹żŃõ»ÆÄʵē×ÓŹ½£ŗ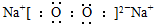 |
C”¢Na+½į¹¹¼ņĶ¼£ŗ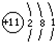 |
| D”¢ÉŁĮæĀČĘųĶØČėäå»ÆŃĒĢśČÜŅŗÖŠ2FeBr2+3Cl2ØT2FeCl3+2 Br2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ŃĒĻõĖįÄĘŹĒŅ»ÖÖŹ³Ę··ĄøƼĮ£¬µ«Ź¹ÓĆŹ±ĘäÓĆĮæŠčŅŖ¼ÓŅŌĻŽÖĘ |
| B”¢²£Į§”¢ĢÕ“É”¢Ė®Äą¶¼ŹĒ¹čĖįŃĪ²śĘ·£¬ŹōÓŚĪŽ»ś·Ē½šŹō²ÄĮĻ |
| C”¢Na2SæɳżČ„·ĻĖ®ÖŠHg2+”¢Pb2+µČÖŲ½šŹōĄė×Ó |
| D”¢ČõĖįŠŌ»ņÖŠŠŌĢõ¼žĻĀ£¬øÖĢśøÆŹ“µÄÕż¼«·“Ó¦Ź½ĪŖ£ŗ4OH--4e-ØTO2+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
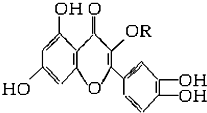 ĢģČ»Ī¬ÉśĖŲP£Ø½į¹¹ČēĶ¼£¬·Ö×Ó½į¹¹ÖŠRĪŖ±„ŗĶĢž»ł£©“ęŌŚÓŚ»±Ź÷»ØĄŁÖŠ£¬ĖüŹĒŅ»ÖÖÓŖŃųŌö²¹¼Į£¬¹ŲÓŚĪ¬ÉśĖŲPµÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©
ĢģČ»Ī¬ÉśĖŲP£Ø½į¹¹ČēĶ¼£¬·Ö×Ó½į¹¹ÖŠRĪŖ±„ŗĶĢž»ł£©“ęŌŚÓŚ»±Ź÷»ØĄŁÖŠ£¬ĖüŹĒŅ»ÖÖÓŖŃųŌö²¹¼Į£¬¹ŲÓŚĪ¬ÉśĖŲPµÄŠšŹöÕżČ·µÄŹĒ£Ø””””£©| A”¢æÉÓėäåĖ®·“Ó¦£¬ĒŅ1moløĆĪļÖŹÓė×ćĮæäåĖ®·“Ó¦ĻūŗÄ6molBr2 |
| B”¢æÉÓėNaOHČÜŅŗ·“Ó¦£¬1moløĆĪļÖŹæÉÓė5molNaOH·“Ó¦ |
| C”¢Ņ»¶ØĢõ¼žĻĀ1moløĆĪļÖŹæÉÓėH2¼Ó³É£¬ŗÄH2×ī“óĮæĪŖ6mol |
| D”¢Ī¬ÉśĖŲPÄÜ·¢ÉśĖ®½ā·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Ė®½ā | B”¢±äŠŌ |
| C”¢ŃĪĪö | D”¢ŃÕÉ«·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢¢Ł | B”¢¢Ś | C”¢¢Ū | D”¢¢Ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com