
”¾ĢāÄæ”æŌŚ25”ꏱ£¬ĆܱÕČŻĘ÷ÖŠX”¢Y”¢ZČżÖÖĘųĢåµÄ³õŹ¼ÅضČŗĶĘ½ŗāÅضČČēĻĀ±ķ£ŗ
ĪļÖŹ | X | Y | Z |
³õŹ¼ÅضČ/mol”¤L-1 | 0.1 | 0.2 | 0 |
Ę½ŗāÅضČ/mol”¤L-1 | 0.05 | 0.05 | 0.1 |
ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£ŗ
A. ·“Ó¦“ļµ½Ę½ŗāŹ±£¬XµÄ×Ŗ»ÆĀŹĪŖ50£„ B. ·“Ó¦æɱķŹ¾ĪŖX+3Y![]() 2Z£¬ĘäĘ½ŗā³£ŹżĪŖ1600 C. Ōö“óŃ¹ĒæŹ¹Ę½ŗāĻņÉś³ÉZµÄ·½ĻņŅĘ¶Æ£¬Ę½ŗā³£ŹżŌö“ó D. øıäĪĀ¶ČæÉŅŌøıä“Ė·“Ó¦µÄĘ½ŗā³£Źż
2Z£¬ĘäĘ½ŗā³£ŹżĪŖ1600 C. Ōö“óŃ¹ĒæŹ¹Ę½ŗāĻņÉś³ÉZµÄ·½ĻņŅĘ¶Æ£¬Ę½ŗā³£ŹżŌö“ó D. øıäĪĀ¶ČæÉŅŌøıä“Ė·“Ó¦µÄĘ½ŗā³£Źż
”¾“š°ø”æC
”¾½āĪö”æ
ŹŌĢāÓɱķæÉÖŖĘ½ŗāŹ±£¬XµÄÅØ¶Č±ä»ÆĮæŹĒ0.05mol/L£¬ZµÄ±ä»ÆĮæŹĒ0.15mol/L£¬ZµÄ±ä»ÆĮæŹĒ0.1mol/L£¬·“Ó¦µÄ»Æѧ¼ĘĮæĻµŹżÖ®±ČµČÓŚÅØ¶Č±ä»ÆĮæÖ®±Č£¬²ĪÓė·“Ó¦µÄn£ØX£© : n£ØY£© : n£ØZ£© = 1:3:2£¬ĖłŅŌ·“Ó¦æÉŅŌ±ķŹ¾ĪŖX+3Y![]() 2Z”£CĻī£¬øĆ·“Ó¦Õż·“Ó¦·½ĻņŹĒĢå»ż¼õŠ”µÄ·“Ó¦£¬Ōö“óŃ¹ĒæĘ½ŗāÓŅŅĘ£¬µ«ŹĒĘ½ŗā³£Źż²»±ä£¬¹ŹCĻī“ķĪó£»AĻī£¬Ę½ŗāŹ±XµÄ×Ŗ»ÆĀŹĪŖ0.05/0.1*100%=50%£¬¹ŹAĻīÕżČ·£»BĻī£¬Ę½ŗā³£ŹżK=£Ø0.12£©/£Ø0.053*0.05£©=1600£¬¹ŹBĻīÕżČ·£»DĻī£¬Ę½ŗā³£ŹżÖ»Óė·“Ó¦±¾ÉķŗĶĪĀ¶ČÓŠ¹Ų£¬øıäĪĀ¶ČæÉŅŌøıä“Ė·“Ó¦µÄĘ½ŗā³£Źż£¬¹ŹDĻīÕżČ·”£×ŪÉĻĖłŹö£¬±¾ĢāÕżČ·“š°øĪŖC”£
2Z”£CĻī£¬øĆ·“Ó¦Õż·“Ó¦·½ĻņŹĒĢå»ż¼õŠ”µÄ·“Ó¦£¬Ōö“óŃ¹ĒæĘ½ŗāÓŅŅĘ£¬µ«ŹĒĘ½ŗā³£Źż²»±ä£¬¹ŹCĻī“ķĪó£»AĻī£¬Ę½ŗāŹ±XµÄ×Ŗ»ÆĀŹĪŖ0.05/0.1*100%=50%£¬¹ŹAĻīÕżČ·£»BĻī£¬Ę½ŗā³£ŹżK=£Ø0.12£©/£Ø0.053*0.05£©=1600£¬¹ŹBĻīÕżČ·£»DĻī£¬Ę½ŗā³£ŹżÖ»Óė·“Ó¦±¾ÉķŗĶĪĀ¶ČÓŠ¹Ų£¬øıäĪĀ¶ČæÉŅŌøıä“Ė·“Ó¦µÄĘ½ŗā³£Źż£¬¹ŹDĻīÕżČ·”£×ŪÉĻĖłŹö£¬±¾ĢāÕżČ·“š°øĪŖC”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøıä0.1mol/L¶žŌŖČõĖįH2AČÜŅŗµÄpH£¬ČÜŅŗÖŠµÄH2A”¢HA-”¢A2-µÄĪļÖŹµÄĮæ·ÖŹż![]() ĖępHµÄ±ä»ÆČēĶ¼ĖłŹ¾[ŅŃÖŖ
ĖępHµÄ±ä»ÆČēĶ¼ĖłŹ¾[ŅŃÖŖ ]”£
]ӣ

ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A. pH=1.2Ź±£¬c(H2A)=c(HA-)
B. lg[K2(H2A)]=-4.2
C. pH =2.7Ź±£¬c(HA-)>c(H2A)=c(A2-)
D. pH=4.2Ź±£¬c(HA-)=c(A2-)=c(H+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜÓ°ĻģĖ®µÄµēĄėĘ½ŗā,²¢Ź¹ČÜŅŗÖŠµÄc(H+)>c(OH-)µÄ“ėŹ©ŹĒ£Ø £©
A. ĻņĖ®ÖŠĶØČėSO2 B. ½«Ė®¼ÓČČÖó·Š
C. Ļņ“æĖ®ÖŠĶ¶ČėŅ»Š”æ齚ŹōÄĘ D. ĻņĖ®ÖŠ¼ÓČėNaCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ĶعżNOx“«øŠĘ÷æɼą²āNOxµÄŗ¬Į棬Ę乤×÷ŌĄķŹ¾ŅāĶ¼ČēĻĀ£ŗ
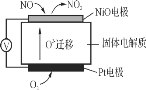
¢ŁPtµē¼«ÉĻ·¢ÉśµÄŹĒ_______(Ģī”°Ńõ»Æ”±»ņ”°»¹Ō”±)·“Ó¦”£
¢ŚŠ“³öNiOµē¼«µÄµē¼«·“Ó¦Ź½£ŗ___________________________________”£
£Ø2£©ĻĀĶ¼ŹĒĄūÓĆ¼×ĶéČ¼ĮĻµē³Ųµē½ā50 mL 2 mol”¤L£1µÄĀČ»ÆĶČÜŅŗµÄ×°ÖĆŹ¾ŅāĶ¼£ŗ
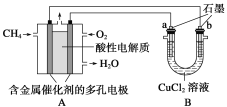
Ēė»Ų“š£ŗ¢Ł¼×ĶéČ¼ĮĻµē³Ųøŗ¼«·“Ó¦Ź½ŹĒ_______________________________________”£
¢Śµ±ĻßĀ·ÖŠÓŠ0.1 molµē×ÓĶعżŹ±£¬________(Ģī”°a”±»ņ”°b”±)¼«ŌöÖŲ________ g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃĒĮņĖįÄĘÖŠÓŠ+4¼ŪµÄĮņ£¬Ėü¼ČÓŠŃõ»ÆŠŌÓÖÓŠ»¹ŌŠŌ,ĻÖÓŠŹŌ¼Į£ŗäåĖ®”¢Na2SČÜŅŗ”¢Na2SO3ČÜŅŗ”¢Ļ”ĮņĖį”¢NaOHČÜŅŗ”¢°±Ė®”£
(1)ŅŖÖ¤Ć÷Na2SO3¾ßÓŠ»¹ŌŠŌ,ӦєÓƵďŌ¼ĮÓŠ______,擵½µÄĻÖĻóŹĒ_______,·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ__________”£
(2)ŅŖÖ¤Ć÷Na2SO3¾ßÓŠŃõ»ÆŠŌ,ӦєÓƵďŌ¼ĮÓŠ_____,擵½µÄĻÖĻóŹĒ________,·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖŅāŅ唣¶ŌÓŚĆܱÕČŻĘ÷ÖŠµÄ·“Ó¦£ŗN2(g)£«3H2(g)![]() 2NH3(g)£¬ŌŚ673 K”¢30 MPaĻĀ£¬n(NH3)ŗĶn(H2)Ėꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
2NH3(g)£¬ŌŚ673 K”¢30 MPaĻĀ£¬n(NH3)ŗĶn(H2)Ėꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ

A. µćaµÄÕż·“Ó¦ĖŁĀŹ±ČµćbµÄŠ”
B. µćc“¦·“Ó¦“ļµ½Ę½ŗā
C. µćd(t1Ź±æĢ)ŗĶµće(t2Ź±æĢ)“¦n(N2)²»Ņ»Ńł
D. µće“¦·“Ó¦“ļµ½Ę½ŗā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI.ĻĀ±ķŹĒŹŅĪĀĻĀ£¬¼øÖÖČõĖįµÄµēĄėĘ½ŗā³£Źż(Ka)ŗĶČõ¼īµÄµēĄėĘ½ŗā³£Źż(Kb):

Ēė»Ų“šĻĀĆęĪŹĢā:
(1)ÓĆÕōĮóĖ®Ļ”ŹĶ0.1mol/LµÄ“×ĖįČÜŅŗ,ĻĀĮŠŃ”ĻīÖŠŅ»¶Ø±äŠ”µÄŹĒ_____
A.c(H+) B.c(H+)”¤c(OH-) C. ![]()
(2)CH3COONH4µÄĖ®ČÜŅŗ³Ź_______(Ń”ĢīĖįŠŌ”±”¢”°ÖŠŠŌ"»ņ”°¼īŠŌ”±)”£
(3)ÅضČĪŖ0.10mol/LÄūĆŹĖįĒā¶žÄĘ(Na2HC6H5O7)ČÜŅŗĻŌĖįŠŌ,Ķعż¼ĘĖćĖµĆ÷ĘäŌŅņ______”£
(4)¹¤ŅµÖŠ³£ÓĆĢ¼ĖįÄųÖʱøŃõ»ÆÄų”£ŅŃÖŖ:Ksp(NiCO3)=1.4”Į10-7£¬µ±Ni,2+Ē”ŗĆĶźČ«×Ŗ»ÆĪŖNiCO3³Įµķ[¼“ČÜŅŗÖŠc(Ni2+)=1”Į10-5mol”¤L-1]Ź±,ČÜŅŗÖŠc(CO32-)=_____mol/L”£
II.(1)ŅŅ“¼ŹĒÖŲŅŖµÄ»Æ¹¤²śĘ·ŗĶŅŗĢåČ¼ĮĻ£¬æÉŅŌĄūÓĆĻĀĮŠ·“Ó¦ÖĘČ”ŅŅ“¼”£
2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) ”÷H=akJ/mol
CH3CH2OH(g)+3H2O(g) ”÷H=akJ/mol
ŌŚŅ»¶ØŃ¹ĒæĻĀ,²āµĆ.ÉĻŹö·“Ó¦µÄŹµŃ鏿¾ŻČēĻĀ±ķ”£

øł¾Ż±ķÖŠŹż¾Ż·ÖĪö:
¢ŁÉĻŹö·“Ó¦µÄa_____0(Ģī"“óÓŚ”±»ņ”°Š”ÓŚ”±)”£
¢ŚŌŚŅ»¶ØĪĀ¶ČĻĀ.ĢįøßĒāĢ¼[¼“![]() ]±Č,Ę½ŗā³£ŹżKÖµ_____(Ģī”°Ōö“ó”±”¢”°¼õŠ””±”¢»ņ"²»±ä”±)”£
]±Č,Ę½ŗā³£ŹżKÖµ_____(Ģī”°Ōö“ó”±”¢”°¼õŠ””±”¢»ņ"²»±ä”±)”£
(2)“߻ƼĮ“ęŌŚµÄĢõ¼žĻĀ,ŌŚ¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠĶ¶ČėŅ»¶ØĮæµÄCOŗĶH2,Ķ¬ŃłæÉÖʵĆŅŅ“¼(æÉÄę·“Ó¦)”£øĆ·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾;

øł¾ŻÉĻĶ¼,Š“³ö·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŌŖĖŲÖÜĘŚ±ķÖŠ£¬Ī»ÓŚµŚ¶žÖÜĘŚµŚ¢öA×åµÄŌŖĖŲŹĒ
A. O B. N C. C D. F
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫“Ö¹č×Ŗ»Æ³ÉČżĀČ¹čĶé£ØSiHCl3£©£¬½ųŅ»²½·“Ó¦Ņ²æÉŅŌÖĘµĆ“Ö¹č”£Ęä·“Ó¦ĪŖ£ŗSiHCl3£Øg£©£«H2£Øg£©![]() Si£Øs£©£«3HCl£Øg£©”£²»Ķ¬ĪĀ¶ČĻĀ£¬SiHCl3µÄĘ½ŗā×Ŗ»ÆĀŹĖę·“Ó¦ĪļµÄĶ¶ĮĻ±Č£Ø·“Ó¦³õŹ¼Ź±ø÷·“Ó¦ĪļµÄĪļÖŹµÄĮæÖ®±Č£©µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
Si£Øs£©£«3HCl£Øg£©”£²»Ķ¬ĪĀ¶ČĻĀ£¬SiHCl3µÄĘ½ŗā×Ŗ»ÆĀŹĖę·“Ó¦ĪļµÄĶ¶ĮĻ±Č£Ø·“Ó¦³õŹ¼Ź±ø÷·“Ó¦ĪļµÄĪļÖŹµÄĮæÖ®±Č£©µÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
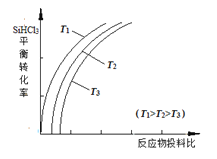
A. øĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦
B. ŗį×ų±ź±ķŹ¾µÄĶ¶ĮĻ±ČÓ¦øĆŹĒ![]()
C. øĆ·“Ó¦µÄĘ½ŗā³£ŹżĖęĪĀ¶ČÉżø߶ųŌö“ó
D. Źµ¼ŹÉś²śÖŠĪŖĢįøßSiHCl3µÄĄūÓĆĀŹ£¬æÉŅŌŹŹµ±Ōö“óŃ¹Ēæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com