
城市使用的燃料,现大多为煤气、液化石油气和天然气。煤气的主要成分是CO和H2的混合气体,它由煤炭与水蒸气在高温下反应制得,故又称水煤气。试回答:
(1)写出制取水煤气的主要化学方程式_____________________________________,该反应是__________反应(填吸热、放热)。
(2)设液化石油气的主要成分为丙烷(C3H8),其充分燃烧后产物为C02和H2O,试比较完全燃烧等质量的C3H8及CO所需的氧气的质量比为:_____________。
(3)1molCH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。煤矿常因瓦斯(CH4)爆炸而引起重大事故,为了避免事故的发生,特别要求矿井通风,严禁烟火,从反应条件的控制分析其理由:
科目:高中化学 来源: 题型:
(8分)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它由煤炭和水蒸气反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式____________________________.
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为
C3H8(g) +5O2(g)== 3CO2(g) + 4H2O(l);△H=–2220.0 kJ·![]() ,
,
又知CO气体燃烧的热化学方程式为:
CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·![]() ,
,
试比较同质量的C3H8和CO燃烧,产生的热量比值约为_________:1。
(3)已知氢气燃烧的热化学方程式为2H2(g)+ O2(g) == 2H2O(l);△H=–571.6 kJ·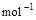 ,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
(4)氢气是未来的能源,除来源丰富之外,还具有的优点是____________________
查看答案和解析>>
科目:高中化学 来源:2010年辽宁省本溪县高中高二暑期补课阶段考试化学试题 题型:填空题
(8分)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它由煤炭和水蒸气反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式____________________________.
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为
C3H8(g) +5O2(g) == 3CO2(g) + 4H2O(l);△H=–2220.0 kJ· ,
,
又知CO气体燃烧的热化学方程式为:
CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ· ,
,
试比较同质量的C3H8和CO燃烧,产生的热量比值约为_________:1。
(3)已知氢气燃烧的热化学方程式为2H2(g) + O2(g) == 2H2O(l);△H=–571.6 kJ· ,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
(4)氢气是未来的能源,除来源丰富之外,还具有的优点是____________________
查看答案和解析>>
科目:高中化学 来源:2010年辽宁省高二暑期补课阶段考试化学试题 题型:填空题
(8分)城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它由煤炭和水蒸气反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式____________________________.
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为
C3H8(g) +5O2(g)
== 3CO2(g) + 4H2O(l);△H=–2220.0 kJ·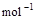 ,
,
又知CO气体燃烧的热化学方程式为:
CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·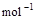 ,
,
试比较同质量的C3H8和CO燃烧,产生的热量比值约为_________:1。
(3)已知氢气燃烧的热化学方程式为2H2(g)
+ O2(g) == 2H2O(l);△H=–571.6 kJ·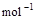 ,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
(4)氢气是未来的能源,除来源丰富之外,还具有的优点是____________________
查看答案和解析>>
科目:高中化学 来源:同步题 题型:判断题
查看答案和解析>>
科目:高中化学 来源: 题型:
城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它由煤炭和水蒸气反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式____________________________.
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为
C3H8(g) +5O2(g) == 3CO2(g) + 4H2O(l);△H=–2220.0 kJ·![]() ,
,
又知CO气体燃烧的热化学方程式为:
CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·![]() ,
,
试比较同质量的C3H8和CO燃烧,产生的热量比值约为_________:1。
(3)已知氢气燃烧的热化学方程式为2H2(g) + O2(g) == 2H2O(l);△H=–571.6 kJ·![]() ,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________:1。
(4)氢气是未来的能源,除来源丰富之外,还具有的优点是____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com