
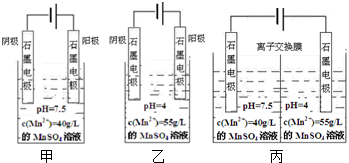
���� ��1�����������ڼ�����������Ũ���ᷴӦ�����Ȼ��̡�������ˮ��
��2�������Խ����У�Mn2+��������MnO4-��NaBiO3����ԭ��Bi3+���и�������������ɣ������������Ϊ�Ϻ�ɫ�����������£�����������Ӱ�����������Ϊ������
��3�������������������ӷŵ磻
�ڸ�������Ũ�ȼ��㣻
���ҳ���������������ʧ�������ɶ������̣������������ӵõ�������������
��4������֪�����������Ϸֱ�õ�����Mn��MnO2��˵�����ʱMn2+��������ʧ���ӣ��������ϵõ��ӣ�
�ڱ��д������ӽ���Ĥ��ֻ������������ͨ����
��5������п�̵�طŵ�ʱ��������Znʧ��������������п�������϶������̵õ�������MnOOH��
��� �⣺��1�����������ڼ�����������Ũ���ᷴӦ�����Ȼ��̡�������ˮ���䷴Ӧ�ķ���ʽΪ��MnO2+2Cl-+4H+$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
�ʴ�Ϊ��MnO2+2Cl-+4H+$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O��
��2��NaBiO3����ǿ�����ԣ���KMnO4������ǿ������Mn2+����Ϊ����������ӣ��и�������������ɣ������������Ϊ�Ϻ�ɫ���÷�Ӧ�����ӷ���ʽΪ��2Mn2++5NaBiO3+14H+=2MnO4-+5Na++5Bi3++7H2O�����������£�����������Ӱ�����������Ϊ�����������Һ�Ϻ�ɫ��ȥ��
�ʴ�Ϊ����Һ��Ϊ�Ϻ�ɫ��2Mn2++5NaBiO3+14H+=2MnO4-+5Na++5Bi3++7H2O�����ɵ�MnO4-��������Һ�б�Cl-��ԭΪMn2+��
��3������������Һ�У����������������ӷŵ�����������
�ʴ�Ϊ��������
����Һ��Mn2+��c��Mn2+��=55g/L������Һ��MnSO4������Ϊ55g/L��0.25L��$\frac{151}{55}$=37.75���ʴ�Ϊ��37.75��
���ҳ���������������ʧ�������ɶ������̣������������ӵõ����������������Ե����������Һ�ĵõ��������̡����������ᣬ�䷽��ʽΪ��MnSO4+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$MnO2��+H2SO4+H2����
�ʴ�Ϊ��MnSO4+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$MnO2��+H2SO4+H2����
��4������֪�����������Ϸֱ�õ�����Mn��MnO2��˵�����ʱMn2+��������ʧ���ӣ��������ϵõ��ӣ�
�ڱ��д������ӽ���Ĥ��ֻ������������ͨ��������˵���Ч�ʣ������Ʊ�������Ŀ���������ܺ���ͣ�
�ʴ�Ϊ���Ʊ�������Ŀ���������ܺ���ͣ�
��5������п�̵�طŵ�ʱ��������Znʧ��������������п�������϶������̵õ�������MnOOH�����طŵ�ʱ���ܷ�ӦʽZn+2MnO2+2H2O=2MnOOH+Zn��OH��2��
�ʴ�Ϊ��Zn+2MnO2+2H2O=2MnOOH+Zn��OH��2��
���� ���⿼���˵���ԭ����ԭ���ԭ����Ӧ�ã���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ��������ͼ���������ע��������������ӵķŵ�˳���Լ��缫����ʽ����д������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
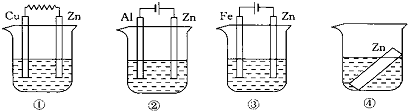
| A�� | �٢ڢۢ� | B�� | �ڢ٢ۢ� | C�� | �ۢ٢ܢ� | D�� | �ڢ٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
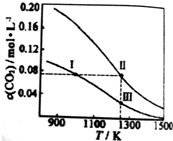
| A�� | ��ӦCO2��g��+c��s��?2CO��g����H��0 | |
| B�� | ��Ӧ���ʣ�V����״̬��V����״̬�� | |
| C�� | ��ϵ��c��CO����c��CO��״̬��2c��CO��״̬�� | |
| D�� | ��ϵ��ѹǿ��2P����״̬��P����״̬��P����״̬�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x=4 | B�� | ƽ��������Ӧ�����ƶ� | ||
| C�� | B��ת���ʽ��� | D�� | C������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������1 L pH=1�Ĵ�����Һ�м�ˮ��������Һ��H+��Ŀ����0.1NA | |
| B�� | 60g�����������Ҵ�����������Ӧ����ַ�Ӧ����ѵ�C-O����ĿΪNA | |
| C�� | ij��ˮ�Ҵ������������Ʒ�Ӧ����5.6 L H2�����Ҵ������й��ۼ�����Ϊ4 NA | |
| D�� | ��֪C2H4��g��+H2��g���TC2H6��g����H=-137.0 kI/mol����ϩ��H2�ӳ�ʱ�ų�68.5 kJ��������Ӧ�����б��ƻ���̼ԭ��֮�乲�õ��Ӷ���ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��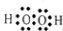 ��
�� ��
�� ��
�� ��
�� ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���䡢��С | B�� | ����С | C�� | ��С������ | D�� | ���䡢���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �������Һ | H2SO4��Һ | KOH��Һ |
| ������Ӧʽ | ||
| ������Ӧʽ | ||
| ��Һ��pH�仯 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com