
向10 mL 0.1 mol·L-1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL。下列叙述正确的是( )
A.x=10时,溶液中有NH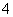 、Al3+、SO
、Al3+、SO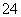 ,且c(NH
,且c(NH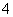 )>c(Al3+)
)>c(Al3+)
B.x=10时,溶液中有NH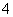 、AlO
、AlO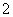 、SO
、SO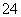 ,且c(NH
,且c(NH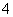 )>c(SO
)>c(SO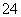 )
)
C.x=30时,溶液中有Ba2+、AlO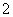 、OH-,且c(OH-)<c(AlO
、OH-,且c(OH-)<c(AlO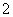 )
)
D.x=30时,溶液中有Ba2+、Al3+、OH-,且c(OH-)=c(Ba2+)
解析 10 mL 0.1 mol·L-1 NH4Al(SO4)2的溶液中,加入等浓度Ba(OH)2溶液时,Ba2+与SO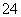 反应,OH-与NH
反应,OH-与NH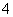 、Al3+反应。当x=10时,NH4Al(SO4)2与Ba(OH)2物质的量相等,Ba2+、OH-反应完毕,SO
、Al3+反应。当x=10时,NH4Al(SO4)2与Ba(OH)2物质的量相等,Ba2+、OH-反应完毕,SO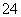 剩一半没有反应,由于Al3+结合OH-的能力大于NH
剩一半没有反应,由于Al3+结合OH-的能力大于NH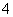 ,故OH-优先与Al3+反应,根据Al3++3OH-===Al(OH)3↓可知OH-不足,Al3+未完全反应,NH
,故OH-优先与Al3+反应,根据Al3++3OH-===Al(OH)3↓可知OH-不足,Al3+未完全反应,NH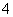 没有与OH-反应,所以溶液中有NH
没有与OH-反应,所以溶液中有NH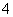 、Al3+、SO
、Al3+、SO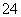 ,且c(NH
,且c(NH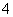 )>c(Al3+),由于NH
)>c(Al3+),由于NH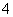 水解导致溶液中c(SO
水解导致溶液中c(SO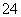 )>c(NH
)>c(NH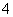 ),故A项正确,B项错误。当x=30时,Al3+转化为AlO
),故A项正确,B项错误。当x=30时,Al3+转化为AlO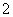 ,NH
,NH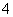 转化为NH3·H2O。由于NH3·H2O的电离导致反应后溶液中c(OH-)大于c(Ba2+)和c(AlO
转化为NH3·H2O。由于NH3·H2O的电离导致反应后溶液中c(OH-)大于c(Ba2+)和c(AlO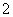 ),故C、D项错误。
),故C、D项错误。
答案 A


科目:高中化学 来源: 题型:
化学实验研究中经常用到定量分析。
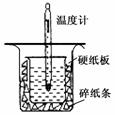 I.取0.55 mol/L的NaOH溶液50mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
I.取0.55 mol/L的NaOH溶液50mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
(1)从右图实验装置看,装置中的一个明显错误是
。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值
会_________,(填“偏大”、“偏小”、“ 不变”)
(3)实验中改用60mL0.50mol·L-1盐酸跟50mL0.55 mol·L-1NaOH 溶液进行反应,与上述实验相比,所求中和热________(填“相等”或“不相等”),简述理由 。
Ⅱ.某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下某一刻度,并记下读数
④移取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
 请回答:
请回答:
(1)以上步骤有错误的是(填编号)________,该错误操作会导致
测定结果(填“偏大”、“偏小”或“无影响”) 。
(2)判断滴定终点的现象是:________________,且半分钟内不变色。
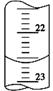
(3)如图是某次滴定时的滴定管中的液面,其读数为 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.在101 kPa时,1 mol H2完全燃烧生成气态水,放出285.8 kJ热量,H2的燃烧热为-285.8 kJ·mol-1
B.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后终止温度
C.在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ·mol-1
D.在稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.31 kJ·mol-1。若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。
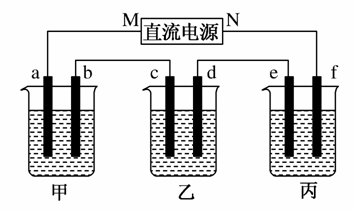
接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,②中c电极质量增加。据此回答问题:
(1)电源的N端为________极;
(2)电极b上发生的电极反应为__________________________;
(3)列式计算电极b上生成的气体在标准状况下的体积:_______
_________________________________________________________;
(4)电极c的质量变化是________g;
(5)电解前后各溶液的酸、碱性大小是否发生变化,并简述其原因:
①溶液_______________________________________________;
②溶液_______________________________________________;
③溶液_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有4种混合溶液,分别由等体积0.1 mol·L-1的2种溶液混合而成:①CH3COONa与HCl;②CH3COONa与NaOH;③CH3COONa与NaCl;④CH3COONa与NaHCO3
下列各项排序正确的是( )
A.pH:②>③>④>①
B.c(CH3COO-):②>④>③>①
C.溶液中c(H+):①>③>②>④
D.c(CH3COOH):①>④>③>②
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数为________________。
在此温度下,将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合。
(1)若所得混合液为中性,且a=2,b=12,则VaVb=________。
(2)若所得混合液的pH=10,且a=2,b=12,则VaVb=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
车用乙醇汽油就是把燃料乙醇和汽油按一定比例混合配形成的车用燃料。结合有关知识,回答以下问题。
(1)乙醇的结构简式为________。汽油是由石油分馏所得的低沸点烷烃,其分子中的碳原子数一般在5~12范围内,如戊烷,其分子式为______________。
(2)乙醇可由含淀粉的农产品如玉米、小麦、薯类等经发酵、蒸馏而得。请写出由淀粉制乙醇的化学方程式:
________________________________________________________________________,
________________________________________________________________________。
(3)若1 mol乙醇充分燃烧生成二氧化碳气体和液态水放热1367 kJ,乙醇燃烧的热化学方程式是:
________________________________________________________________________________________________________________________________________________。
(4)车用乙醇汽油被称为环保燃料,其原因是________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关阳离子的说法中错误的是( )
①阳离子都是由一个金属原子失去电子而形成的 ②非金属原子不能形成阳离子 ③阳离子的电子排布一定与稀有气体元素原子相同 ④阳离子的价态不会大于其原子的最外层电子数 ⑤阳离子都是稳定结构,不会再失去电子
A.①④ B.②④
C.①②③ D.①②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com