
随着环境污染的加重和人们环保意识的加强,生物降解材料逐渐受到了人们的关注。以下是PBA (—种生物降解聚酯高分子材料)的合成路线:

己知:①烃A的相对分子质量为84,核磁共振氢谱显示只有1组峰,不能使溴的四氯化碳溶液褪色。
②化合物C中只含一个官能团。
③R1CH=CHR2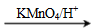 R1COOH+R2COOH
R1COOH+R2COOH
④
(1)由A生成B的反应类型为_________。
(2)由B生成C的化学方程式为__________。
(3)E的结构简式为______________________。
(4)F的名称为______________(用系统命名法);由D和生成PBA的化学方程式为_______________;若PBA的平均聚合度为70,则其平均相对分子质量为___________。
(5)E的同分异构体中能同时满足下列条件的共有_____种(不含立体异构)。
①链状化合物 ②能发生银镜反应 ③氧原子不与碳碳双键直接相连
其中,核磁共振氢谱显示为2组峰,且峰面积比为2:1的是_________(写结构简式)。
(6)若由1.3—丁二烯为原料(其他无机试剂任选)通过三步制备化合物F,其合成路线为:___________________。
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源:2016-2017学年河南省漯河市高二3月月考化学试卷(解析版) 题型:选择题
下列物质:①甲烷、②乙烯、③聚乙烯、④苯、⑤乙醇、⑥苯酚、⑦乙醛,即能使酸性高锰酸钾溶液褪色又能与溴水发生反应使之褪色的是
A. ②③⑥⑦ B. ②⑤⑥⑦ C. ②⑥⑦ D. ③⑥⑦
查看答案和解析>>
科目:高中化学 来源:2017届河南省洛阳市高三第二次统一考试(3月)理综化学试卷(解析版) 题型:简答题
NO2与SO2能发生反应:NO2+SO2 SO3+NO,某研究小组对此进行相关实验探究。
SO3+NO,某研究小组对此进行相关实验探究。
(1)已知:2NO(g)+O2(g)  2NO2(g) △H=-113.0 kJ• mol-1
2NO2(g) △H=-113.0 kJ• mol-1
2SO2(g)+O2(g)  2SO3(g) △H=-196. 6 kJ• mol-1
2SO3(g) △H=-196. 6 kJ• mol-1
则NO2(g)+SO2(g)  SO3(g)+N0(g) △H= ________.
SO3(g)+N0(g) △H= ________.
(2)实验中,尾气可以用碱溶液吸收。NaOH溶液吸收N02时,发生的反应为:
2NO2+2OH- =NO2- +NO3- +H2O,反应中形成的化学键是________(填化学键的类型);用NaOH溶液吸收少量SO2的离子方程式为____________。
(3)在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。 部分实验结果如图所示:
①当容器内_______(填标号)不再随时间的变化而改变时,可以不断反应达到了化学平衡状态。
a.气体的压强
b.气体的平均摩尔质量
c.气体的密度
d.NO2的体积分数
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是________。
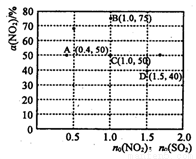
③若A点对应实验中,S02(g)的起始浓度为c0 mol•L-1 ,经过t min达到平衡状态,该时段化学反应速率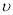 (N02)= _________mol•L-1•min -1.
(N02)= _________mol•L-1•min -1.
④图中C、D两点对应的实验温度分别为Tc和Td,通过计算判断::Tc_____Td(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考化学试卷(解析版) 题型:选择题
下列事实不能说明非金属性Cl﹥I的是( )
A. KClO3+I2=KIO3+Cl2 B. Cl2+2I-=2Cl-+I2
C. 酸性:HClO4﹥HIO4 D. 氧化性:Cl2﹥I2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考化学试卷(解析版) 题型:选择题
当光束通过下列分散系:①有尘埃的空气 ② 稀硫酸 ③蒸馏水④ 豆浆,能观察到丁达尔效应的是( )
A. ①② B. ②③
C. ①④ D. ②④
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三下学期第一次统测理综化学试卷(解析版) 题型:选择题
常温下,某溶液X由Fe3+、SO42-、Cu2+、Na+、CO32-、Al3+中的几种离子组成。取少量待测液滴加KSCN溶液,溶液变红;另取少量待测滴加NaOH溶液至pH=4后过滤,向滤液中继续滴加NaOH溶液至过量时又得到沉淀W和溶液Y。可能用到的数据如下表所示,下列说法正确的是
沉淀物 | Fe(OH)3 | Cu(OH)2 | Al(OH)3 |
开始沉淀的pH | 1.9 | 4.7 | 3.4 |
沉淀完全的pH | 3.2 | 6.7 | 4.7 |
A. 该温度下Ksp[Fe(OH)3]=1×10-14.6
B. W主要含有 Cu(OH)2和Al(OH)3
C. 溶液X中一定含有Cu2+、Fe3+和SO42-
D. 取溶液Y进行焰色反应,可判断溶液X中是否含有Na+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:填空题
(1)两个试剂瓶各盛装质量相同的浓硫酸和浓硝酸,分别敞口放置一段时间后,两溶液质量关系为m(硫酸)_____ m(硝酸)(填“>”、“<”或“=”),由于浓硫酸和浓硝酸都具有强氧化性,所以冷的浓硫酸和浓硝酸都可以用_____(写金属名称)制容器盛放。
(2)制备CuSO4和Cu(NO3)2
①下列有四种制备Cu(NO3)2的途径,其中最佳途径是(选填字母)___
a. Cu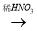 Cu(NO3)2
Cu(NO3)2
b. Cu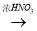 Cu(NO3)2
Cu(NO3)2
c. Cu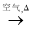 CuO
CuO 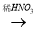 Cu(NO3)2
Cu(NO3)2
d. Cu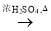 CuSO4
CuSO4  Cu(NO3)2
Cu(NO3)2
② 向稀硫酸溶液中加入铜粉,然后通入热空气,可制得硫酸铜溶液,则发生反应的离子方程式为___________________________________。
(3)向200mL2mol/LHNO3溶液中加入足量铜粉,充分作用后,有m1g固体不溶物,继续 加入100mL 1mol/L硫酸溶液,充分作用后,还有m2g固体不溶物,则 m1 ________ m2(填“>”、“<”或“=”),两者质量相差g_____(若两者相等,则此问不答)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:选择题
在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡。然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如图所示。下列说法正确的是( )
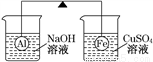
A. 铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡
B. 铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,溶液蓝色变浅,杠杆右边下沉
C. 反应后去掉两烧杯,杠杆仍平衡
D. 右边球上出现红色,左边溶液的c(OH-)增大
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三实验班第六次月考理综化学试卷(解析版) 题型:选择题
已知常温下在溶液中可发生如下两个离子反应Ce4++Fe2+=Fe3++ Ce3+ ,Sn2+ + 2Fe3+ = 2Fe2+ + Sn4+。由此可以确定Fe2+、Ce3+、Sn2+ 三种离子的还原性最强和最弱的离子分别是
A.Sn2+ 和Ce3+ B.Sn2+ 和Fe2+
C.Ce3+和Sn2+ D.Fe2+和Ce3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com