
【题目】将粗盐溶于水后,其中的杂质可用过滤的方法除去的是
A.Mg2+B.Ca2+C.SO42-D.泥沙
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
如图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:
(1)该浓硫酸中H2SO4的物质的量浓度为
(2)某学生欲用上述浓硫酸和蒸馏水配制250mL物质的量浓度为0.4molL﹣1的稀硫酸,该学生需要量取上述浓硫酸进行配制.
(3)为配制(2)中的稀硫酸,下列可供选用的仪器中,一定用到的是(填编号),配制过程中还缺少的仪器是(填写仪器名称)
①玻璃棒;②胶头滴管;③量筒;④药匙;⑤圆底烧瓶;⑥天平;⑦烧杯;⑧普通漏斗
(4)取上述配制好的硫酸溶液50mL与足量的铝反应,所得溶液中c(Al3+)=(忽略溶液体积的变化),检验溶液中SO42﹣存在的方法:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学知识在生产和生活中有着重要的应用。下列说法中正确的是
A.依据铝热反应原理,能发生反应2Al+3MgO![]() 3Mg+Al2O3
3Mg+Al2O3
B.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
C.硫酸铁和明矾都可用于净水
D.Na2CO3可以与胃酸反应,可用Na2CO3治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,Y的体积分数与时间关系如图II所示.则下列结论正确的是
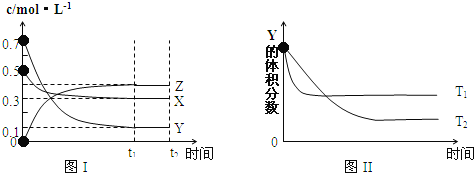
A. 该反应的热化学方程式为:X(g)+3Y(g)![]() 2Z(g);△H>0
2Z(g);△H>0
B. 若其它条件不变,升高温度,正、逆反应速率均增大,X的转化率减小
C. 达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动
D. 达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)完全燃烧0.1mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9g,浓碱液增重17.6g.该烃的化学式 , 并写出其所有可能的结构简式: .
(2)两种气态烃以任意比例混合,在120℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体仍为10L.则两气态烃的分子的组成要符合的条件是 .
(3)如图所示,将浸透了石蜡油(分子中含有17个碳原子以上的液态烷烃混合物)的矿渣棉放置在硬质试管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸气通过碎瓷片表面,发生反应,可得到一定量的气体生成物,用该生成物进行如下实验: 
①生成的气体通入酸性KMnO4溶液中,溶液褪色.
②生成的气体通入Br2的CCl4溶液中,溶液褪色.
③用排水法收集一试管气体,点燃,燃烧时火焰明亮,有黑烟产生(甲烷燃烧时火焰为淡蓝色,无烟).
根据以上现象思考:
A.用其最简单的同系物为例,写出②的反应方程式: .
B.碎瓷片的作用是 .
C.产生黑烟的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学反应:Fe +CuSO4 = FeSO4 + Cu,可以设计出一种原电池。该原电池工作时:
A.Fe 为正极 B.Cu 为负极
C.负极上发生氧化反应 D.正极上发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应 CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如下图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如下图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )

A. 反应 CO2(g)+C(s)![]() 2CO(g)的 ΔS>0、 ΔH<0
2CO(g)的 ΔS>0、 ΔH<0
B. 体系的总压强p总:p总(状态Ⅱ) <2p总(状态Ⅰ)
C. 体系中 c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D. 逆反应速率v逆: v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是
A. 中子数为20的氯原子: ![]() Cl B. 硫离子的结构示意图:
Cl B. 硫离子的结构示意图:
C. N2H4的电子式:![]() D. 丙烯的结构简式:CH2CHCH3
D. 丙烯的结构简式:CH2CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以软锰矿(主要成分为MnO2,还有少量FeO、Fe2O3、MgO和Al2O3杂质)为原料制备高锰酸钾的流程如下图:

(1) “酸浸”需要加热的目的是__________,此过程中发生反应的离子方程式是______________。(任写一条)
(2) “熔融”过程中,MnO2被KC1O3氧化成K2MnO4。
①该反应的化学方程式为_____________________。
②加入KC1O3应过量的原因除了提高MnO2利用率,还有_________________.
③将适量KClO3和KOH混合均匀后在坩埚内高温反应,应选用坩埚为__________。(选填序号)
a.石英坩埚 b.铁坩埚 c.氧化铝坩埚
(3)己知:①MnO42-只存在于强碱环境(pH>13.5)中,当pH降低时,MnO42-会歧化为MnO4-和MnO2;②饱和碳酸钾溶液的pH约为12.3,饱和碳酸氢钾溶液的pH约为8.8;③相关物质的溶解度曲线如下图。

请补充完整由浸取液制备KMnO4晶体的实验方案:向浸取液中缓缓通入CO2,_____________,低温供干得KMnO4晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com