
【题目】下列装置一定能证明2Ag++2I-=2Ag+I2能否自发进行的是
A.  B.
B. 
C. 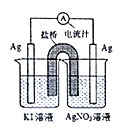 D.
D. 
【答案】C
【解析】
A、反应产生黄色沉淀,证明碘化钾与硝酸银反应生成碘化银和硝酸钾,不符合,选项A不选;B、两个电极为石墨电极不能发生自发的氧化还原反应,无法形成原电池,无法证明2Ag++2I-=2Ag+I2能否自发进行,不符合,选项B不选;C、左边银电极上碘离子失电子产生碘单质,右边银离子在电极上得电子析出银,能证明2Ag++2I-=2Ag+I2能否自发进行,符合,选项C选;D、碘化银连接电源的正极氢氧根离子失电子产生氧气,银电极连接电源负极银离子得电子产生银单质,证明电解硝酸银产生银、氧气和硝酸,无法证明2Ag++2I-=2Ag+I2能否自发进行,不符合,选项D不选。答案选C。


科目:高中化学 来源: 题型:
【题目】下列对能源的看法不合理的是
A. 生物能是一种可再生能源,有广泛的前景
B. 太阳能、氢能、核能、地热能都属于新能源
C. 我国人口众多、资源相对匮乏、环境承载能力较弱,因此要建设节约型社会
D. 我国化石能源丰富且属于可再生能源,想用多少就用多少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量10.0g含有少量中性易溶杂质的样品,配成500mL待测溶液。 用0.100mol![]() L-1硫酸滴定,写出该中和反应的热化学方程式______________________(中和热ΔH=-57.3 kJ/mol)。
L-1硫酸滴定,写出该中和反应的热化学方程式______________________(中和热ΔH=-57.3 kJ/mol)。
(2)将该烧碱样品配成500mL待测溶液需要的玻璃仪器有________________________。
(3)滴定过程中,眼睛应注视_________________________,若用酚酞作指示剂达到滴定终点颜色变化是______________________________________________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________molL-1,烧碱样品的纯度是___________。
滴定次数 | 待测溶液 体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(5)下列实验操作会对滴定结果产生什么后果?(填“偏高”“偏低”或“无影响”)
① 观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果____________。
② 若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知M2On2-可与R2-作用,R2-被氧化为R单质,M2On2-的还原产物中M为+3价;又知c(M2On2-) =0.3mol/L的溶液100mL 可与c(R2-)=0.6mol/L的溶液150mL恰好完全反应,则n值为()
A.4 B.5 C.6 D.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的有( )
①标准状况下,20 g重水(D2O)中含有的电子数为10NA
②0.5 mol Fe2+与足量的H2O2溶液反应,转移NA个电子
③将2 mol NO和1 mol O2混合后,体系中的分子总数为3NA
④常温下,0.4 mol SiO2所含的共价键数目为1.6NA
⑤2 mol·L-1碳酸钠溶液中Na+的数目是2NA
⑥1 mol氯气溶解在水中得到的新制氯水中氢离子的数目是NA
⑦22.4 L的N2的共用电子对数为3NA
A. 2个 B. 3个 C. 4个 D. 5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应中的说法错误的是( )
A. 化学反应中有物质变化也有能量变化。
B. 化学键断裂吸收能量,化学键生成放出能量。
C. 需要加热的化学反应不一定是吸热反应。
D. 如图所示的反应为放热反应。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质可以实现一步转化的是( )
A. N2→NO2→HNO3→NH4ClB. Al→Al2O3→Al(OH)3→AlCl3
C. Cu→CuCl2→Cu(OH)2→CuOD. Si→SiO2→H2SiO3→NaSiO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com