
| A. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| B. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-═BaSO4↓ | |
| D. | 常温下,将铁片置于浓硝酸中:Fe+6HNO3═Fe(NO3)3+3NO2↑+3H2O |
分析 A.氨水过量反应生成亚硫酸铵;
B.磁性氧化铁溶于足量稀硝酸反应生成硝酸铁、一氧化氮和水;
C.漏写铵根离子与碱的反应;
D.常温下铁遇到浓硝酸发生钝化.
解答 解:A.用氨水吸收过量二氧化硫,离子方程式:2NH3•H2O+SO2═2NH4++SO32-十H2O,故A正确;
B.将磁性氧化铁溶于足量稀硝酸中的离子反应为3Fe3O4+NO3-+28H+═9Fe3++14H2O+NO↑,故B错误;
C.向(NH4)2SO4溶液中加入适量Ba(OH)2,离子方程式:2NH4++2OH-+Ba2++SO42-═BaSO4↓+2NH3.H2O,故C错误;
D.常温下铁遇到浓硝酸发生钝化,形成致密氧化膜,阻止反应进行,故D错误;
故选:A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意反应物用量对反应的影响,题目难度中等.


科目:高中化学 来源: 题型:填空题
| 物质 | 摩尔质量 | 物质的量 | 质量 | 分子或 离子数目 |
| SO2 | 64g/mol | 2mol | 128g | 1.204×1024 |
| SO${\;}_{4}^{2-}$ | 96g/mol | 10mol | 960g | 6.02×1024 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ①②③ | C. | ③④⑥ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )可用作防腐剂,对酵母菌和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得.以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
)可用作防腐剂,对酵母菌和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得.以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
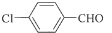 +2Cu(OH)2 $\stackrel{△}{→}$
+2Cu(OH)2 $\stackrel{△}{→}$ +Cu2O↓+2H2O;
+Cu2O↓+2H2O; ,其核磁共振氢谱中不同化学环境的氢的峰面积比为1:2:2:1,它与足量NaOH溶液反应的方程式为
,其核磁共振氢谱中不同化学环境的氢的峰面积比为1:2:2:1,它与足量NaOH溶液反应的方程式为 +3NaOH $\stackrel{△}{→}$
+3NaOH $\stackrel{△}{→}$ +HCOONa+2H2O.
+HCOONa+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某有机物的结构如图所示,这种有机物具有的性质是( )
某有机物的结构如图所示,这种有机物具有的性质是( )| A. | 只有①④ | B. | 只有①④⑤ | C. | ①②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池反应的化学方程式为:CH3CH2OH+O2═CH3COOH+H2O | |
| B. | 检测时,电解质溶液中的 H+向负极移动 | |
| C. | 若有 0.4 mol 电子转移,则在标准状况下消耗 4.48 L 氧气 | |
| D. | 正极上发生的反应为:O2+4e-+2H2O═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
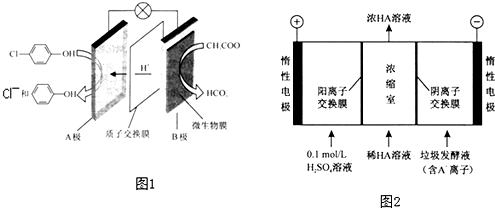
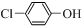 )的废水可以通过构成微生物电池除去,其原理如图1所示.
)的废水可以通过构成微生物电池除去,其原理如图1所示. -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-.
-OH+Cl-.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)在烷烃分子中,每增加一个碳原子,1mol 烷烃完全燃烧需要多消耗氧气(填字母)B.
(1)在烷烃分子中,每增加一个碳原子,1mol 烷烃完全燃烧需要多消耗氧气(填字母)B.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com