
̼�Ļ���������������������������ء�
��1����״���£���11.2LCO2ͨ��100mL 1mol/L��NaOH��Һ�У�������Һ������Ũ���ɴ�С��˳��Ϊ___________������Һ������Ũ�ȷ���������е�ʽ:
��c(OH-)=2c(H2CO3)+______��
��c(H+)+c(Na+)=_________��
��2����ͼ��1mol NO2��1molCO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��___________

��3����һ���¡������ܱ������з�����Ӧ��Ni(s)+4CO(g) Ni(CO)4(g)��
Ni(CO)4(g)�� H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99.9���ĸߴ���������˵����ȷ����________ (����ĸ���)��
H<0�����ø÷�Ӧ���Խ�����ת��Ϊ���ȴ�99.9���ĸߴ���������˵����ȷ����________ (����ĸ���)��
A������Ni���������CO��ת���ʣ�Ni��ת���ʽ���
B����С�����ݻ���ƽ�����ƣ� H��С
H��С
C����Ӧ�ﵽƽ�����CO�ٴδﵽƽ��ʱ��CO�������������
D����4v��[Ni(CO)4]=v��(CO)ʱ�������л�������ܶȲ���ʱ������˵����Ӧ�Ѵﻯѧƽ��״̬
��4�������Ѵ���������ķ�Ӧ���̣���Ҫ�������¼�����Ӧ����������Ϊ25�桢1.01��105Pa�ⶨ����
��CH3OCH3(g)+H2O(l) 2CH3OH(l) ��H����24.52kJ/mol
2CH3OH(l) ��H����24.52kJ/mol
��CH3OH(l)+H2O(l) CO2(g)+3H2(g) ��H����49.01kJ/mol
CO2(g)+3H2(g) ��H����49.01kJ/mol
��CO(g)+H2O(l) CO2(g)+H2(g) ��H����41.17kJ/mol
CO2(g)+H2(g) ��H����41.17kJ/mol
��CH3OH(l) CO(g)+2H2(g) ��H����90.1kJ/mol
CO(g)+2H2(g) ��H����90.1kJ/mol
��ҵ�����в�ò�ͬ�¶��¸�������������������ת���ʵĹ�ϵ����ͼ��ʾ��


������Ϊ��Ӧ���Ƶ�����¶�ӦΪ___________��
A��300��350�� B��350��400�� C��400��450�� D��450��500��
�����¶ȴﵽ400���Ժ�������CO2�Լ�����ͬ�ı仯�������Խ��ͣ���CO��H2�������Ҳ�Լ�����ͬ�ı仯�������ߣ��������ܵ�ԭ����___________������Ӧ�Ļ�ѧ����ʽ��ʾ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶�3��ѧҵˮƽ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ҹ��״��ĺ����������塢�������缫����ˮΪ�������Һ�������е�����������Ӧ��������������ܷ�ӦΪ��4Al��3O2��6H2O��4Al(OH)3�������жϲ���ȷ���ǣ� ��
A. ��ع���ʱ�������������ص���������
B. �õ�ع���ʱ����ת��Ϊ��ѧ��
C. ���缫������״���������������ĽӴ����
D. �õ��ͨ��ֻ��Ҫ��������Ϳɼ���ʹ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�����и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ�������й�������ȷ����
A. 30gNO��30gSiO2�к��е���ԭ������ΪNA
B. 0.5L2.0mol��L-1NaHSO3��Һ�к��е�HSO3-��ĿΪNA
C. ��״���£�5.6LN2��������H2��Ӧ����NH3ת�Ƶĵ�����Ϊ1.5NA
D. ��״���£�11.2LNH3��11.2LHCl��Ϻ����������з�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ƹ��и���3��������������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
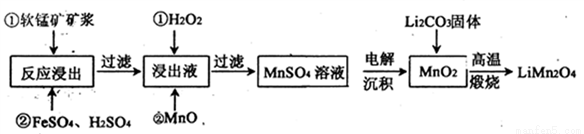
����﮵��������������ﮣ�LiMn2O4)����ȡ���㷺ʹ�õ�LiCoO2����ҵ����ij���̿�(��Ҫ�ɷ�ΪMnO2��ͬʱ������������������ȵ������Ϊԭ���Ʊ�����﮵��������£�
�й����ʵ��ܶȻ�����
���� | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
Ksp | 8.0��10-16 | 4.0��l0-38 | 4.5��10-33 | 1.9��l0-13 |
(1)��֪��﮵�طŵ������ĵ缫��ӦΪ��LiMn2O4+e-+Li+= Li2Mn2O4����﮵����������������У���Ԫ�صĻ��ϼ�Ϊ________��
(2)�����У�FeSO4��������_______��MnO��������_________������Һ�е�pHΪ6ʱ����Һ�����������ӵ�Ũ��Ϊ___________��
(3)������ͼװ�õ�⣬���ӽ���Ĥ�����طָ�Ϊ�����Һ������ң����ҵ���Һ�ֱ�Ϊ��������Һ���Ƶõ���������Һ�����������е���ҺΪ________����������MnO2�����ڵ缫�ϣ��õ缫��ӦʽΪ_________��
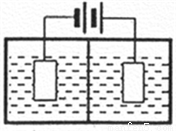
(4)��������װ���е���������Һ��Ϊ���̿�Ŀ������������������������ᣬ��һ����������̿�Ľ�����Ӧ�������MnO2��Ӧ�����ʱ��Fe3+�ȷŵ�����Fe2+��������Fe2+������е� MnO2��Ӧ���ܶ���ʼ��ֱ�����е�MnO2��ȫ��������Fe2+�����MnO2��Ӧ�����ӷ���ʽΪ__________��
(5)д������������������﮵Ļ�ѧ����ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ƹ��и���3��������������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 0.01 mol��L-1��ˮ�У�Cl2��Cl-��ClO-��������Ŀ֮�ʹ���0.01NA
B. ����ȼ�ϵ����������22.4 L����ʱ,�������ĵ����������ĿΪ2NA
C. 0.1mol Cu��������Ũ������ȫ��Ӧ��,��Һ��Cu2+��ĿΪ0.1NA
D. 2.0 g D2O�к��е�����������������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�г���������ظ���3��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ۼ���ϩ�������(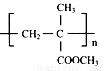 )��д����ΪPMMA���׳��л�����������˵���д������
)��д����ΪPMMA���׳��л�����������˵���д������
A. �ϳ�PMMA�ĵ����Ǽ���ϩ��ͼ״�
B. �ۼ���ϩ������ķ���ʽ�ɱ�ʾΪ(C5H8O2��n
C. �ۼ���ϩ����������л��ɷ��Ӻϳɲ���
D. ����ϩ�����[CH2=C(CH3)COOCH3]��̼ԭ�ӿ��ܶ�����ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
�������������У��������ϼ��������ڡ�
(1)����һ�ֻ��ý��������н�ǿ�Ļ�ԭ�ԡ�
�ٽ������ڸ�������������������Ӧ��2Al��Fe2O3��Al2O3��2Fe����Ϊ���ȷ�Ӧ���� ��˫���ŷ���ʾ����ת�������____________________��
���ܷ�����������ʢװNaOH��Һ��________(��ܡ����ܡ�)��
(2)��þ�����Ļ���ﹲ0.2 mol������200 mL 4 mol��L��1��������Һ�У�Ȼ���ٵμ�2 mol��L��1��NaOH��Һ����ش��������⣺
�����ڵμ�NaOH��Һ�Ĺ����У���������m�����NaOH��Һ�����V�仯�����ͼ��ʾ����V1��160 mLʱ���������ĩ��n (Al)��________________________mol��
��0��V1�η����ķ�Ӧ�����ӷ���ʽΪ______________________________��
�����ڵμ�NaOH��Һ�Ĺ����У���ʹMg2����Al3���պó�����ȫ�������NaOH��Һ�����V(NaOH)��_____________mL��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����( )
A. �Ȼ�����Һ�ڵ��������µ����Na+��Cl?
B. ����ˮ���ܵ����H+�Ļ����ﶼ����
C. �Ȼ�������ˮ���ܵ��磬��Һ̬�Ȼ��ⲻ�ܵ���
D. ������ǿ����Һ�������ƶ�������Ŀһ���ȵ�����������Һ�������ƶ�������Ŀ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ����и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
MnO2�dz������������������ͻ��Ե缫���ϡ�
(1)��ҵ�ϣ��Զ��Բ���Ϊ�缫�����MnSO4��Һ��������ϡ���ᣩ�Ʊ�MnO2��д�������ĵ缫��Ӧʽ��___________��
(2)��֪�����Ȼ�ѧ����ʽ(K����ƽ�ⳣ��)��
��MnCO3(s) MnO(s)+CO2(g) ��H1 K1
MnO(s)+CO2(g) ��H1 K1
��2MnO(s)+O2(g) 2MnO2(s) ��H2 K2
2MnO2(s) ��H2 K2
��2MnCO3(s)+O2(g) 2MnO2(s)+2CO2(g) ��H3 K3
2MnO2(s)+2CO2(g) ��H3 K3
��H3=______(�á�H1����H2��ʾ) K3=_______(��K1��K2��ʾ����
(3)��Ӧ���ڵ������������Է����У����H2______0(�>����<����=��)��
(4)���ܱ�������Ͷ��������MnCO3�����������·�����Ӧ:MnCO3(s) MnO(s)+CO2(g)
MnO(s)+CO2(g)
��H>0����һ���¶��£��ﵽƽ��״̬ʱp(CO2)=2a MPa��

�� �¶ȡ�ѹǿ��MnCO3�ֽ��ʵ�Ӱ����ͼ��ʾ���Ƚϣ�L1____L2(�>����<����=��)��
�� �����¶Ȳ��䣬���������������ԭ����2������p(CO2)�ı仯��Χ��______��
�� �����¶Ȳ��䣬���������ѹ����ԭ����һ�룬�ﵽ��ƽ��ʱ����������-���������__(����ţ���
A.ƽ�ⳣ��K B.c(CO2) C.n(CO2) D.m(MnCO3)
(5)�����¶��£����ݻ�Ϊ2L�ĺ����ܱ������м���������MnCO3(s)��5molO2��������Ӧ��2MnCO(s)+O2(g) 2MnO2(s)+2CO2(g)��CO2��ƽ������0.1mol• L-1��min-1����10min�ﵽƽ��״̬���������¸÷�Ӧ��ƽ�ⳣ��KΪ_______��
2MnO2(s)+2CO2(g)��CO2��ƽ������0.1mol• L-1��min-1����10min�ﵽƽ��״̬���������¸÷�Ӧ��ƽ�ⳣ��KΪ_______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com