
| m |
| M |
| 1840g×98% |
| 98 |


科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
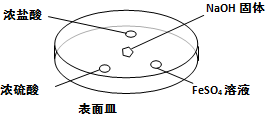
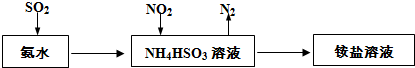
查看答案和解析>>
科目:高中化学 来源: 题型:
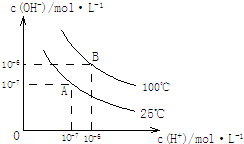 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解法精炼粗铜,用纯铜作阴极 |
| B、在镀件上电镀锌,用锌作阳极 |
C、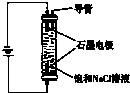 用如图装置生产家用消毒液(NaClO) |
D、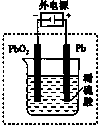 用如图装置为铅蓄电池充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶解度 | B、物质的量浓度 |
| C、质量分数 | D、摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、处理废水时可加入明矾作为混凝剂,以吸附水中的杂质 |
| B、废弃的塑料、金属、纸制品是可回收资源,玻璃是不可回收资源 |
| C、酸雨样品露天放置一段时间,酸性增强,是由于雨水中某种成分被氧化 |
| D、工业上可利用铝热反应原理制备高熔点金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com