
(一)5mol的CO2与8mol的SO2的分子数比是 ;原子数比是 ;质量比是 。
(二)KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯。其反应可表述为:
KClO3+ HCl(浓) → KCl+ ClO2+ Cl2+ H2O
(1)配平以上化学方程式(化学计量数填入划线上)。
(2) ClO2是反应的 (填氧化或还原)产物。
(3)浓盐酸在反应中显示出来的性质是(填写号码)
①还原性 ②氧化性 ③酸性 ④碱性
(4)反应产生0.1 mol Cl2,则转移的电子的物质的量为 mol
(5)ClO2具有很强的氧化性,因此可被用来做消毒剂,若ClO2作消毒剂后其自身转化为Cl-,则其消毒的效率(以单位质量得到电子数表示)是Cl2的 倍(保留2位小数)。
(共9分)(一)5:8 5:8 55:128
(二)(1) 2 KClO3+ 4 HCl(浓) → 2 KCl+ 2 ClO2+ 1 Cl2+ 2 H2O
(2) 还原 (3)①③ (2分)
(4)0.2 (5)2.63倍(保留2位小数)。
解析试题分析:(一)气体的分子数之比等于物质的量之比,所以5mol的CO2与8mol的SO2的分子数比是5:8,CO2与SO2均是三原子分子,所以原子数之比也为5:8,质量之比等于物质的量之比乘以摩尔质量之比等于55:128.
(二)⑴根据氧化还原反应中得失电子守恒规律及观察法配平方程式即可,2 KClO3+ 4 HCl(浓) → 2 KCl+ 2 ClO2+ 1 Cl2+ 2 H2O
⑵分析反应,ClO2是KClO3得电子被还原后的产物,所以是还原产物
⑶浓盐酸失去电子被氧化为氯气,同时该反应中有KCl 、H2O生成,还起到了酸的作用,答案选①③
⑷由2HCl~Cl2得产生0.1 mol Cl2,应转移0.2mol电子
⑸由Cl2~2HCl,知每克氯气得电子为2/71g,由 ClO2~Cl-,知每克ClO2得电子为5/67.5g,后者是前者的(5/67.5)/(2/71)=2.63倍
考点:考查阿伏伽德罗定律的应用、化学方程式的配平、产物的判断、电子的转移数目、反应物作用的判断、计算


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:单选题
现有质量分数为15%的食盐溶液20 g,质量分数为40%的食盐溶液15 g,另有足够多的食盐固体和水,要配制质量分数为20%的食盐溶液30 g。
(1)试选择多种可能的配制方法(至少四种)。
(2)若要求尽可能多地使用现有的食盐水,应如何配制?
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关化学用语表示正确的是( )
| A.甲酸甲酯的结构简式:CH2O |
B.Na+的.结构示意图: |
C.质子数为53、中子数为78的碘原子: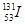 |
D.CO2的电子式为: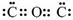 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列表示对应化学反应或过程的离子方程式正确的是
| A.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| B.碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
C.用石墨作电极电解AlCl3溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| D.亚硫酸氢钠溶液显酸性:NaHSO3=Na++H++ SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,30 L pH=11的Na2CO3溶液中含有的OH-数为0.03NA |
| B.用含有0.1 mol FeCl3的饱和溶液制得的氢氧化铁胶体中,胶粒数等于0.1NA |
| C.25℃时,pH=13的1LBa(OH)2溶液中含有的OH-数为0.2NA |
| D.100 mL 12 mol·L-l浓盐酸与足量MnO2加热反应,产生的氯气分子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是(设NA表示阿伏加德罗常数的值)( )
| A.80℃时,1 L pH=1的硫酸溶液中,含有0.2NA个H+ |
| B.4.6 g Na完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1NA |
| C.标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA |
| D.300 mL 2 mol·L-1蔗糖溶液中所含分子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
3 g镁铝合金与100 mL稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4 g,则原硫酸的物质的量浓度为( )
| A.1 mol·L-1 | B.1.5 mol·L-1 |
| C.2 mol·L-1 | D.2.5 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法正确的是( )
| A.9.2 g NO2气体中含有分子数目为0.2NA |
| B.标准状况下,2.24 L SO3中含有氧原子数目为0.3NA |
C.2 g 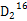 O中含中子、质子、电子数目均为NA O中含中子、质子、电子数目均为NA |
| D.标准状况下2.24 L Cl2通入足量水中或NaOH溶液中,转移电子数目均为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com