
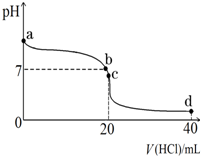
 ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ��Ϊ�ⶨ�����Ũ����ʵ�����н�������ʵ�飺�����������գ�
ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ��Ϊ�ⶨ�����Ũ����ʵ�����н�������ʵ�飺�����������գ�| ʵ���� | NaOH��Һ����������mL�� | ����������Һ�������mL�� |
| 1 | 22.62 | 20.00 |
| 2 | 22.72 | 20.00 |
| 3 | 22.80 | 20.00 |
���� ��2���ٸ��ݴ���Һ�м����̪����ҺΪ��ɫ����Ӧ��ȫ���������ƹ�������Һ��ɺ�ɫ�жϴﵽ�յ�����
�����ж����ݵĺ����ԣ������NaOH��Һ�����Ȼ�������NaOH��Һ��ƽ�������Ȼ�����c��HCl��=$\frac{c��NaOH����V��NaOH��}{V��HCl��}$���㣻
�۸���c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������������V��������Ӱ�죬�Դ��ж�Ũ�ȵ���
��3����һˮ�ϰ�Ϊ������ʣ���Һ�в��ֵ����笠����Ӻ����������ӣ�
��b������������С��20mL����ˮ�������ݴ��ж���Һ�е�������ɣ�
��c��ʱ��ˮ������ǡ�÷�Ӧ�����Ȼ����Һ�������ε�ˮ��ԭ��������غ��ж���Һ�и�����Ũ�ȴ�С��
��� �⣺��2���������м����̪����Һ��ʾ��ɫ�����ᷴӦ��ȫ��������������Һ����Һ��ʾ��ɫ�����Եζ��յ�Ϊ���һ��NaOH��Һ�������ƿ����Һǡ�ó��ֺ�ɫ���Ұ�����ں�ɫ����ȥ��
�ʴ�Ϊ�����һ��NaOH��Һ�������ƿ����Һǡ�ó��ֺ�ɫ���Ұ�����ں�ɫ����ȥ��
�����εζ����ݶ�����Ч�ģ����ı�Һ��ƽ�����Ϊ��$\frac{22.62+22.72+22.80}{3}$mL=22.713mL���������Ũ�ȸ���c��HCl��=$\frac{c��NaOH����V��NaOH��}{V��HCl��}$=$\frac{0.10mol/L��0.022713L}{0.02L}$��0.11mol/L��
�ʴ�Ϊ��0.11mol/L��
��A���ζ��յ����ʱ���Ӷ��������V������ƫС������c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������֪c�����⣩ƫ�ͣ���A��ȷ��
B����ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ô���������Һ��ϴ������ҺŨ��ƫС������Һ�����ʵ���ƫС�����V������ƫС������c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������֪c�����⣩ƫ�ͣ���B����
C����ƿˮϴ��δ�����V��������Ӱ�죬����c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������֪c�����⣩��Ӱ�죬��C����
D��1molNaOH��40g����1molHCl��1molNa2CO3��106g����2molHCl�����������NaOH��Na2CO3�����ᷴӦ��NaOH���ĵ�����࣬����������ᷴӦʱ����Ҫ�Ļ���Na2CO3��NaOH����Һ�϶࣬����c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������֪c�����⣩ƫ�ߣ���D��ȷ��
E��NaOH����Һ����������е�CO2��Ӧ������Na2CO3���������غ㣬��V��������Ӱ�죬����c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������֪c�����⣩���䣬��E����
F����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ�����V������ƫ����c�����⣩=$\frac{c����ע����V������}{V�����⣩}$��������֪c�����⣩ƫ�ߣ���F��ȷ��
�ʴ�Ϊ��DF��
��3����һˮ�ϰ�Ϊ�������Һ�д��ڵ���ƽ�⣺NH3•H2O?NH4++OH-��
��Ϊ��NH3•H2O?NH4++OH-��
��b��ʱ�������������Һ���С��20mL����ʱ��ˮ������������Ϊ��NH4Cl��NH3?H2O��
����NH4Cl��NH3?H2O��
��c��ʱ������20mL���ᣬ��ˮ������ǡ����ȫ��Ӧ�����Ȼ����Һ������笠����Ӳ���ˮ�⣬��Һ��ʾ���ԣ���c��H+����c��OH-�������ݵ���غ㣺��NH4+��+c��H+��=c��Cl-��+c��OH-���ɵã���Cl-����c��NH4+������Һ�и�����Ũ�ȴ�СΪ��c��Cl-����c��NH4+����c��H+����c��OH-����
�ʴ�Ϊ��c��Cl-����c��NH4+����c��H+����c��OH-����c��Cl-��+c��OH-����
���� ���⿼������к͵ζ��������������Һ�����жϣ���Ŀ�Ѷ��еȣ�ע���������������Һ�е����ʼ������ʡ������غ�͵���غ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
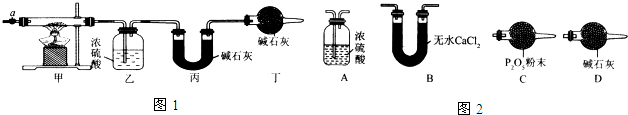
| ��װ�õ�����/g | ��װ�õ�����/g | |
| ����ǰ | 80.00 | 62.00 |
| ���Ⱥ� | 80.36 | 62.88 |
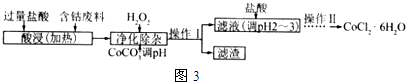
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 |
| ��ʼ������pH�� | 2.3 | 7.5 | 7.6 | 3.4 |
| ��ȫ������pH�� | 4.1 | 9.7 | 9.2 | 5.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
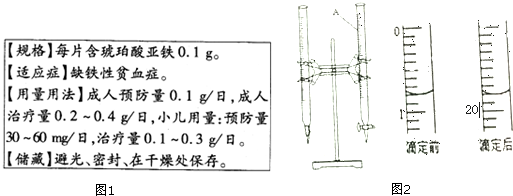
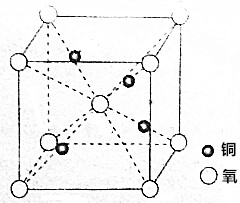 ͭ��һ�����������մ�Ϳɫ�ȷ�������ҪӦ�ã����ľ�����ͼ��ʾ��
ͭ��һ�����������մ�Ϳɫ�ȷ�������ҪӦ�ã����ľ�����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �Թ�1 | �Թ�2 | |
| ʵ������ | ��ɫ�ܿ� | ��ɫ���� |
| ��ɫʱ��/s | 4�� | 31�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
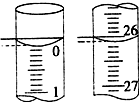 ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ���̪��ָʾ��������д���пհף�
ijѧ������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ���̪��ָʾ��������д���пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
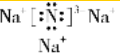 ��
�� ��д����һ���εĵ���ʽ
��д����һ���εĵ���ʽ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2+CuO�TCu+H2O | B�� | 2Na2O2+2H2O�T4NaOH+O2�� | ||
| C�� | H2+Cl2�T2HCl | D�� | 2NaOH+Cl2�TNaCl+NaClO+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 6�� | C�� | 4�� | D�� | 3�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com