
甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,
戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列 判断正确的是( )
判断正确的是( )
 A.金属性:甲>乙>丁
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙和庚的原子核外电子数相差13
D.乙的单质在空气中燃烧生成只含离子键的化合物
科目:高中化学 来源: 题型:
银制器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可
进行如下处理:在铝质容器中加入食盐溶液,再将变黑的的银器浸入该溶液中,一段时间后发现黑色会褪
去。下列说法正确的是( )
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al + 3Ag2S = 6Ag + Al2S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.SiO2制成的纤维,由于导电能力强而被用于制造光缆
B.用一束光线通过氯化钠溶液和蛋白质溶液,能看到相同的现象
C.SO2和Cl2通入品红溶液,品红均褪色,说明两者的漂白原理相同
D.浓硝酸具有强氧化性,能使铝钝化,故常用铝罐车运输冷的浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素的原子序数依次增大,上述元素中只有一种金属元素。A、B同周期,
化合物AB2、DB2均是可使澄清石灰水变浑浊的气体。又已知C、E的单质均可溶于NaOH溶液,且C与
NaOH溶液反应可产生气体。
(1)写出C、D、E三种元素的名称:
C.________,D________,E________。
(2)写出AB2使澄清石灰水变浑浊的化学方程式:
________________________________________________________________________。
(3)写出C、E的单质分别与NaOH溶液反应的离子方程式:
______________________________________,_ _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素
周期表中相对位置如图所示。若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
A.X的最常见气态氢化物的水溶液显酸性
B.最高价氧化物对应水化物的酸性W比Z强
C.Z的单质与氢气反应较W剧烈
D.X的原子半径小于Y
查看答案和解析>>
科目:高中化学 来源: 题型:
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2
剧烈化合并发生爆炸。则下列判断正确的是
A.非金属性:Z<T<X
B.R与Q的电子数相差26
C.气态氢化物稳定性:R <T<Q
D.最高价氧化物的水化物的酸性:T>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项叙述中,正确的是 ( )
A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素
C.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同
D.24Cr原子的电子排布式是1s22s22p63s23p63d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①为纪念著名天文学家哥白尼,国际纯粹与应用化学联合会将112号元素的符号定为“Cn”,汉语名为“鎶”;②合理利用核能符合“低碳经济”的要求,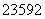 U是核反应堆的重要原料;③锂被誉为“高能金属”,制取锂的原料是β锂辉矿(主要成分是LiAlSi2O6和少量钙、镁杂质)。下列有关对上述表述所涉及元素的说法正确的是 ( )
U是核反应堆的重要原料;③锂被誉为“高能金属”,制取锂的原料是β锂辉矿(主要成分是LiAlSi2O6和少量钙、镁杂质)。下列有关对上述表述所涉及元素的说法正确的是 ( )
A.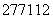 Cn的原子核内中子数与核外电子数之差为55
Cn的原子核内中子数与核外电子数之差为55
B.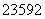 U和
U和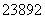 U是同位素,核反应属于化学变化
U是同位素,核反应属于化学变化
C.40Ca2+与18O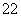 具有相同的电子数
具有相同的电子数
D.Si2O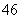 中质子总数为80
中质子总数为80
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com