
 、
、 、
、 ;比烃A少2个碳原子的同系物有4种同分异构体.
;比烃A少2个碳原子的同系物有4种同分异构体. 分析 (1)0.2molCxHy→1.2molCO2+1.2molH2O,由原子守恒分析;
(2)若烃A能使溴水褪色,说明A分子中含有碳碳双键,在催化剂作用下与H2加成生成,其加成产物分子中含有4个甲基,据此可判断A的结构简式;比烃A少2个碳原子的同系物为含有4个C的单烯烃,即为丁烯,根据同分异构体的书写原则写出丁烯的同分异构体.
解答 解:(1)0.2molCxHy→1.2molCO2+1.2molH2O,由原子守恒可知:x=$\frac{1.2mol}{0.2mol}$=6,y=$\frac{1.2mol×2}{0.2mol}$=12,则烃A的分子式为:C6H12,
故答案为:C6H12;
(2)由催化剂作用下与H2发生加成反应,其加成产物经测定分子中含有4个甲基,则生成 或
或 ,则对应的烯烃可能为
,则对应的烯烃可能为 、
、 、
、 ;
;
比烃A少2个碳原子的同系物分子式为C4H8,该物质可能是正丁烯或异丁烯,结构简式为:CH2=CHCH2CH3,CH3CH=CHCH3(顺反异构2种),CH2=C(CH3)3,所以满足条件的有机物有4种同分异构体,
故答案为: 、
、 、
、 ;4.
;4.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握同分异构体的书写原则,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应中NF3是氧化剂,H2O是还原剂 | |
| B. | NF3在潮湿空气中泄漏会产生无色气体 | |
| C. | 反应中还原剂与氧化剂的物质的量之比为1:2 | |
| D. | 若反应中生成0.1 mol HNO3,则反应共转移0.1 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
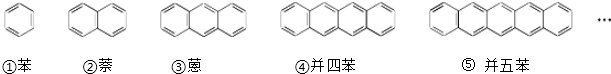
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式CH2CH2 | |
| B. | 甲基的电子式: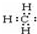 | |
| C. | 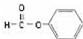 官能团为-COOH 官能团为-COOH | |
| D. | 4-甲基-3-乙基-2-己烯的结构简式为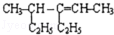 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用超临界二氧化碳代替氟利昂可减轻对臭氧层的破坏 | |
| B. | 超临界二氧化碳由CO2分子构成 | |
| C. | 用超临界二氧化碳溶解物质后,可在常温常压下使二氧化碳挥发除去 | |
| D. | 超临界二氧化碳是新合成的一种物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com