
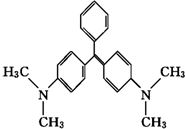
 孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸.其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )
孔雀石绿是化工产品,具有较高毒性,高残留,容易致癌、致畸.其结构简式如图所示.下列关于孔雀石绿的说法正确的是( )| A. | 孔雀石绿的分子式为C23H25N2 | |
| B. | 1 mol孔雀石绿在一定条件下最多可与6 mol H2发生加成反应 | |
| C. | 孔雀石绿属于芳香族化合物 | |
| D. | 孔雀石绿苯环上的一氯取代物有6种 |
分析 A.孔雀石绿的分子中含有23个C原子、26个H原子、2个N原子;
B.孔雀石绿的分子中含有2个苯环和3个C=C键;
C.含有苯环,属于芳香族化合物;
D.含有2个苯环,根据对称结构分析.
解答 解:A.孔雀石绿的分子中含有23个C原子、26个H原子、2个N原子,故分子式为C23H26N2,故A错误;
B.孔雀石绿的分子中含有2个苯环和3个C=C键,2mol苯环共与6mol氢气发生加成反应,3molC=C能与3mol氢气发生加成反应,则1mol孔雀石绿在一定条件下最多可与9molH2发生加成反应,故B错误;
C.含有苯环,属于芳香族化合物,故C正确;
D.孔雀石绿苯环上共有3+2种H原子,如图所示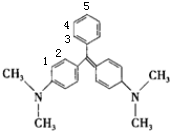 ,孔雀石绿苯环上的一氯取代物有5种,故D错误.
,孔雀石绿苯环上的一氯取代物有5种,故D错误.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目难度中等,本题易错点为A和D,注意分子式的判断以及等效氢原子的判断.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | NaHCO3溶液中加入盐酸:CO32-+2H+═H2O+CO2↑ | |
| C. | 向硫酸溶液中加入Ba(OH)2溶液:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 偏铝酸钠溶液中通入过量二氧化碳:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正常人血液内Kw=10-14 | |
| B. | 由题给数据可算得正常人血液的pH约为7.4 | |
| C. | 正常人血液中存在:c(HCO3-)+c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) | |
| D. | 当过量的碱进入血液中时,只发生HCO3-+OH-=CO32-+H2O的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 每个去甲肾上腺素分子中含有3个酚羟基 | |
| B. | 1mol去甲肾上腺素分子在一定条件下可以和4molH2发生加成反应 | |
| C. | 1mol去甲肾上腺素最多能与含3mol Br2的浓溴水发生取代反应 | |
| D. | 去甲肾上腺素能与氢氧化钠溶液反应,但不能与盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl分子的电子式H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$]- | |
| B. | 乙炔分子的结构式CH≡CH | |
| C. | H2O分子的比例模型 | |
| D. | 甲烷分子的球棍模型 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某课外兴趣小组欲利用如图所示装置自制氢氧燃料电池.
某课外兴趣小组欲利用如图所示装置自制氢氧燃料电池.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 10ml | B. | 30ml | C. | 50ml | D. | 70ml |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com