
【题目】燃烧8.88g某有机物生成CO2和H2O,将燃烧后的气体通过浓H2SO4,浓H2SO4质量增加10.8g,剩余气体通过NaOH溶液,溶液质量增加21.12g。有机物蒸汽密度为3.3g/L(标准状况)。
(1)通过计算写出有机物的分子式。____
(2)若该物质与金属钠反应能放出H2,写出该有机物可能的结构简式。____
【答案】C4H10O CH3CH2CH2CH2OH、CH3CH2CHOHCH3
【解析】
充分燃烧8.88g该有机物,浓硫酸增重10.8g为水的质量,NaOH溶液增重21.12g为生成的二氧化碳的质量,计算二氧化碳和水的物质的量,计算分子中C、H原子数目,再结合质量守恒判断氧原子及数目,据此确定化合物的最简式,有机物的蒸汽密度为3.3g/L,则相对分子质量为3.3×22.4=74,最后根据相对分子质量和最简式写出分子式。
浓硫酸增重10.8g为水的质量,n(H2O)= ![]() =0.6mol,n(H)=2n(H2O)=1.2mol,m(H)=1.2mol×1g/mol=1.2g;
=0.6mol,n(H)=2n(H2O)=1.2mol,m(H)=1.2mol×1g/mol=1.2g;
NaOH溶液增重21.12g为生成二氧化碳的质量,则n(CO2)=![]() =0.48mol,n(C)=n(CO2)=0.48mol,m(C)=0.48mol×12g/mol=5.76g,m(H)+m(C)=1.2g+5.76g=6.96g<8.88g
=0.48mol,n(C)=n(CO2)=0.48mol,m(C)=0.48mol×12g/mol=5.76g,m(H)+m(C)=1.2g+5.76g=6.96g<8.88g
所以含有氧原子,m(O)=8.88g6.96g=1.92g,n(O)=![]() =0.12mol,N(C):N(H):N(O)=0.48mol:1.2mol:0.12mol=4:10:1,故最简式为C4H10O,
=0.12mol,N(C):N(H):N(O)=0.48mol:1.2mol:0.12mol=4:10:1,故最简式为C4H10O,
有机物的蒸汽密度为3.3g/L,则相对分子质量为3.3×22.4=74,则分子式为C4H10O,
答案为: C4H10O,
(2)由有机物的分子式为C4H10O可知其为醇或醚,又知该物质与金属钠反应能放出氢气,故为醇,其有两种同分异构体,可能的结构简式为:
CH3CH2CH2CH2OH和CH3CH2CHOHCH3;
答案为:C4H10O;CH3CH2CH2CH2OH、CH3CH2CHOHCH3;


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g) ΔH=-akJ/mol,已知(a、b、c均大于零),下列说法正确的是( )
2HI(g) ΔH=-akJ/mol,已知(a、b、c均大于零),下列说法正确的是( )

A.反应物的总能量低于生成物的总能量
B.断开1molH—H键和1molI—I键所需能量大于断开2 molH—I键所需能量
C.断开2mol H—I键所需能量约为(c+b+a)kJ
D.向密闭容器中加入2molH2和2molI2,充分反应后放出的热量等于2akJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在200mL5mol/L稀硝酸中加入19.2g铜粉,待充分反应,判断下列说法正确的是(忽略反应前后溶液体积的变化)( )
A.反应中转移电子的物质的量为0.6NA
B.标准状况下,产生NO2气体的体积为4.48L
C.反应后,H+的物质的量浓度为1.0mol/L
D.被还原的HNO3的物质的量为0.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果醋是一种常见的有机酸,其结构简式为

(1)苹果醋中含有的官能团的名称是___、___;
(2)苹果醋的分子式为___;
(3)1mol苹果醋与足量金属钠反应,能生成标准状况下的氢气___L;
(4)苹果醋可能发生的反应是___。
A.与NaOH溶液反应
B.与氢气发生加成反应
C.与乙酸在一定条件下酯化
D.水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)。
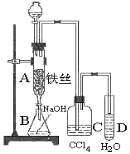
(1)写出A中反应的化学方程式_____。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是____。
(3)C中盛放CCl4的作用是___。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入___,现象是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙、丁、戊五种烃,已知他们是C2H6、C3H6、C2H2、C6H6、C6H12(环己烷),实验现象如下:
①甲、乙能使溴水因化学反应而褪色;②0.5mol甲能与1molH2生成丙,丙不能使溴水和酸性高锰酸钾溶液褪色;③戊可由丁在一定条件下与氢气反应得到。④比乙少一个碳原子的相邻同系物可以在一定条件下和H2O反应得到W,W和醋酸反应会生成一种有香味的油状液体。
(1)这五种烃分别是:甲是____(写电子式);乙是____(写结构简式);丙是____(写结构式);丁是____(写名称)。
(2)写出下列化学方程式:
乙和溴水的反应:______。
实验室制备甲的反应:______。
④中制得香味油状液体的反应:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】玻璃是一种重要的传统无机非金属材料。
(1)普通玻璃又称为钠玻璃,试写出生产普通玻璃过程中发生反应的化学方程式:_____________,_______________。
(2)实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用离子方程式表示):______________;玻璃试剂瓶不能盛放氢氟酸的原因是(用化学方程式表示):______________。
(3)有一种特殊玻璃为钾玻璃,其热膨胀系数较小,较难熔化,较难受化学药品的侵蚀,可用于制作一般的化学仪器。现以石英砂、苛性钾、熟石灰为原料,熔制钾玻璃,质量比为75:28:37(假定这些原料不含杂质),试用氧化物的形式表示该钾玻璃的组成________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组溶液,当后一种溶液逐滴加入到一定量的前一种溶液中并稍过量,其溶液的导电性(I表示导电能力)与后一种溶液的质量(m)的函数关系符合下图的是

A. 澄清石灰水、碳酸钠溶液
B. 硝酸银溶液、氯化钠溶液
C. 盐酸、氢氧化钠溶液
D. 稀硫酸、氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色固体粉末,由FeCl3、CaCO3、Na2SO4、KCl、Ba(NO3)2中的几种物质组成,取样品进行如下实验(假设下列过程中,能反应的物质之间的反应恰好完全):

(1)步骤①所用分离方法叫做___,要从步骤②所得“无色溶液”中提取溶剂,所用分离方法叫做___。
(2)写出实验过程中发生化学反应的离子方程式①___;②___。
(3)固体粉末中一定不存在的物质是(填化学式,下同)___;不能确定是否存在的物质是___。
(4)将固体粉末可能的组成填入下表(可以不填满,也可以再补充)。___
序号 | 化学式 |
Ⅰ | |
Ⅱ | |
(5)设计一个实验,进一步确定混合物的组成,简述实验操作、现象和结论。___
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com