
| A、60mL | B、45mL |
| C、30mL | D、75mL |
| 1.68L |
| 22.4L/mol |
| 0.3mol |
| 4mol/L |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
| A、C60是一种新型化合物 |
| B、C60分子内含有离子键 |
| C、C60在纯氧中充分燃烧后只生成唯一产物CO2 |
| D、C60的摩尔质量为720 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.4g | B、4.8g |
| C、2.4g | D、1.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:
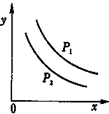 反应:2L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响如图所示:(图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.)据此可判断( )
反应:2L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响如图所示:(图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.)据此可判断( )| A、上述反应的△H小于0 |
| B、上述反应的△H大于0 |
| C、2+a>b |
| D、2+a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③② |
| C、③①② | D、③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al-Mg合金 |
| B、Al-Cu-Mg-Mn-Si合金 |
| C、Al-Si合金 |
| D、表面的氧化铝膜的纯铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com