
【题目】将钠、铝混合物共1.0g投入适量水中充分反应,并测生成H2的量,若混合物中钠与铝的物质的量之比为x,如图为生成H2的物质的量随x的变化关系示意图(随着x的不断增大,产生H2的物质的量越来越接近b1).以下判断不正确的是 ( )
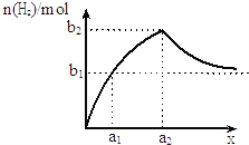
A.a1=![]() B.a2=1C.b1=
B.a2=1C.b1= ![]() D.b2=
D.b2=![]()
【答案】A
【解析】
发生反应有:2Na + 2H2O = 2NaOH + H2 ↑,2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑,开始时铝过量,随着x增大,即钠的量逐渐增大,生成氢气的量开始时会逐渐增大,钠、铝的物质的量相等时,即a2 = 1,生成氢气的量达到增大,之后随着钠的量的增加;生成氢气的量会逐渐减小,成氢气的物质的量,据此进行解答。
A、根据分析可以知道,a1时铝过量,生成氢气量b1与全部是钠时生成的氢气量是一样
的,由此求得![]() ,
,
设钠的物质的量为y mol,此时铝过量,结合反应方程式可以知道参加反应的铝的物质
的量也是ymol,根据电子守恒可得:0.5y + 1.5y = ![]() ,计算得出:
,计算得出:![]() ,
,
则混合物中铝的物质的量为: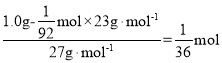 ,
,
则![]() ,故A错误;
,故A错误;
B、根据分析可以知道,当铝和钠的物质的量相等时,生成氢气的量最大,此时a2 = 1,故B正确;
C、当1.0 g完全为钠时,生成氢气的量为![]() ,故C正确;
,故C正确;
D、当钠和铝的物质的量相等时,生成氢气的量为b2,设此时铝和钠的物质的量
都是x mol,则![]() ,计算得出:x = 0.02,则生成氢气的物质的量为:
,计算得出:x = 0.02,则生成氢气的物质的量为:![]() ,故D正确;
,故D正确;
答案为A。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:
【题目】已知某反应A(g)+B(g)=C(g)+D(g),反应过程中的能量变化如图所示,回答下列问题。
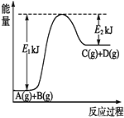
(1)该反应是_____(填“吸热”或“放热”)反应,该反应的ΔH=________kJ/mol (用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量______(填“一定高”“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使反应速率增大,则E1和E2的变化是:E1_______,E2________ΔH______ (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸丁酯的装置如图。下列对该实验的认识正确的是( )
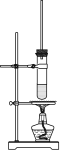
A.采用空气浴加热,石棉网可以避免局部温度过高
B.试管上方长导管的作用是让反应产生的气体逸出
C.反应结束后混合液下层呈油状且有果香味
D.欲提纯乙酸丁酯,需使用水、氢氧化钠溶液洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Fe+6H2SO4(浓) ![]() Fe2(SO4)3+3SO2↑+6H2O。某学习小组对铁丝(含杂质碳)与浓硫酸反应后的产物进行探究。
Fe2(SO4)3+3SO2↑+6H2O。某学习小组对铁丝(含杂质碳)与浓硫酸反应后的产物进行探究。
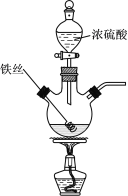
Ⅰ.溶液探究
(1)将反应后的溶液稀释,取稀释液,滴加NaOH溶液,观察到___现象时,证明有Fe3+存在。为进一步判断溶液中是否存在Fe2+,可另取稀释液少许,滴加___(选填编号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.KMnO4酸性溶液
(2)为判断反应停止后硫酸是否有剩余,制定的实验方案为:测定稀释液的pH。请对此实验设计进行评价。____。
Ⅱ.气体探究
(3)将产生的气体依次通过品红溶液和澄清石灰水,观察到:品红溶液褪色、澄清石灰水变浑浊。是否___(填写“是”或“否”)能据此判断除SO2外,反应后气体中还含有CO2?请说明理由___。
最后逸出的气体具有可燃性,推测该气体为H2,理由是___(用离子方程式表示)。
(4)收集混合气体336mL(已折算成标准状况),通入足量的氯水中,发生反应:SO2+Cl2+2H2O=H2SO4+2HCl。滴加足量BaCl2溶液,生成的沉淀经过滤、洗涤、干燥、称量,测得质量为2.330g。则混合气体中SO2的体积分数为___。(精确至小数点后第二位)
(5)将上述混合气体直接通入BaCl2溶液,未见明显现象,放置一段时间后发现有少许浑浊,分析其中的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.在一定温度和压强下,各种气态物质体积大小由分子间距离决定
B.相同温度时,CO2和N2O若体积相同,则它们的质量一定相同
C.100g浓度为18mol/L的浓硫酸中加入等质量的水稀释浓度大于9mol/L
D.14 mol/L的H2SO4溶液的溶质质量分数为80%,那么7 mol/L的H2SO4溶液的溶质质量分数将大于40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的局部X、Y、Z、W均为短周期元素,其原子序数之和为47:
X | |||||
Y | Z | W |
(1)X、Y、Z、W的元素符号依次为_______、________、_______、__________(以下所有问题均用元素符号回答);
(2)X和Y的化合物中的两种微粒均达到了8电子稳定结构,该化合物的电子式为_____;将该化合物的固体溶于足量W的气态氢化物水溶液中,生成两种盐该反应的离子方程式为______________,生成的两种盐的电子式为__________、_____________;
(3)Z的氧化物为_________(填酸性、碱性、两性、不成盐)氧化物,Y、Z、W的最高价氧化物对应的水化物两两之间反应的化学方程式为:![]() __________________________________;
__________________________________;![]() ___________________________;
___________________________;![]() ________________________.
________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种有机物Q(![]() )与P(
)与P(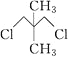 ),下列有关它们的说法中正
),下列有关它们的说法中正
确的是( )
A.二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3∶1
B.二者在NaOH醇溶液中均可发生消去反应
C.一定条件下,二者在NaOH溶液中均可发生取代反应
D.Q的一氯代物只有1种、P的一溴代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为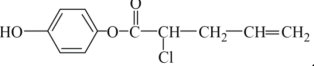 ,其不可能发生的反应有( )
,其不可能发生的反应有( )
①加成反应 ②取代反应 ③消去反应 ④氧化反应 ⑤水解反应 ⑥与氢氧化钠反应 ⑦与稀盐酸反应
A.只有⑦B.①④⑥C.③⑤⑦D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空:
(1)写出电解饱和食盐水的离子方程式________________。
(2)离子交换膜的作用为____________________。
(3)精制饱和食盐水从图中________位置补充,氢氧化钠溶液从图中________位置流出。(选填“a”、“b”、“c”或“d”)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com