
【题目】医用外科口罩中过滤层所用材料是熔喷聚丙烯,具有阻隔部分病毒和细菌的作用,口罩生产中还需使用环氧乙烷进行灭菌。下列说法正确的是
A.熔喷聚丙烯的链节为CH2=CHCH3
B.熔喷聚丙烯可以使溴的四氯化碳溶液褪色
C.废弃的医用外科口罩属于可回收垃圾
D.2CH2=CH2+O2![]() 2
2 是一种最理想的“原子经济性反应”
是一种最理想的“原子经济性反应”
科目:高中化学 来源: 题型:
【题目】利用含多糖淀粉的物质可以生产醋酸。下面是生产醋酸的流程,根据流程回答下列问题:
![]()
![]()
![]() ―→
―→![]() ―→
―→![]() ―→
―→![]()
B是日常生活中常见的有特殊香味的有机物,在有些饮料中含有B。
(1)写出淀粉的分子式___,C中官能团的名称是__。
(2)B→C的反应类型是___(填字母)。
A.取代反应 B.加成反应 C.氧化反应 D.还原反应
(3)写出C完全燃烧的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新科技研究成果表明磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的循环寿命,该电池放电时的反应为![]() 。某磷酸铁锂电池的切面如下图所示。下列说法不正确的是( )。
。某磷酸铁锂电池的切面如下图所示。下列说法不正确的是( )。
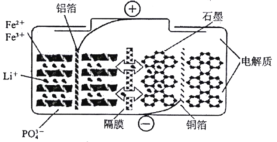
A.放电时,电池负极反应为:![]()
B.充电时,阳极上发生的反应为:![]()
C.放电时,Li+脱离石墨,经电解质嵌入负极
D.充电时,电子从电源负极流出经铜箔流入阴极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某石油化工产品X的转化关系如图所示
![]()
(1)X的结构简式_______
(2)写出转化关系中生成Z、W的化学方程式:_______
(3)上述转化过程中涉及的反应类型有_______
a 取代反应 b 还原反应 c 氧化反应 d 加成反应
(4)写出符合条件的W的同分异构体的结构简式_______
a.能与碳酸氢钠溶液反应 b.分子中有两个甲基
Ⅱ.有机化合物与极性试剂发生取代反应的反应原理可以用下面的通式表示:
![]()
(δ+、δ-表示该基团带一定正或负电性)
写出下列反应的化学方程式:
(1)乙醇跟氢溴酸反应: _______。
(2)碘甲烷跟CH3COONa反应: ______。
(3)溴乙烷跟NaHS反应: ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所给图形回答下列问题:
⑴图表示容器中气体粒子的示意图,图中“![]() ”和“
”和“![]() ”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是______,可表示氯化氢(HCl)分子的是______,可表示一氧化碳和氧气的混合气体的是______(填序号)。
”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是______,可表示氯化氢(HCl)分子的是______,可表示一氧化碳和氧气的混合气体的是______(填序号)。
|
|
|
|
A | B | C | D |
⑵如图是水分子在一定条件下分解的示意图,从中获得的信息不正确的是______(填序号)。
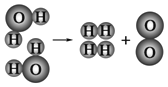
A 生成1mol O2需断开4mol H—O共价键
B 水分解后生成氢气和氧气的分子数比为2:1
C 水分解过程中,分子的种类不变
D 水分解过程中,原子的数目不变
⑶表各图中的小球代表原子序数从1—18元素的原子实![]() 原子实是原子除最外层电子后剩余的部分
原子实是原子除最外层电子后剩余的部分![]() ,小黑点代表未用于形成共价键的最外层电子,短线代表共价键.下列各图表示的结构与化学式一定不相符的是______(填序号)。
,小黑点代表未用于形成共价键的最外层电子,短线代表共价键.下列各图表示的结构与化学式一定不相符的是______(填序号)。
A | B | C |
|
|
|
NH3 | CO2 | CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气,将多余的氯气用100 mL 1.7mol/L的NaOH溶液完全吸收。对吸收后的溶液进行分析化验,测知c(OH-)=0.1mol/L (不考虑反应前后溶液的体积变化) 。ClO-和ClO3-的物质的量浓度之比为5∶1。请回答:
(1)吸收氯气消耗的NaOH的物质的量为_______________mol。
(2)被氧化的氯气的物质的量为_______________mol,被还原的氯气的物质的量为 _______________mol。
(3)若采用二氧化锰和浓盐酸共热的方法制氯气,制备尾气中的氯气所消耗的二氧化锰的质量为_______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素中电负性最大的为_________(填元素符号)。
(2)下列关于CH4和CO2的说法不正确的是_________(填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是非极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp2
(3)在Ni基催化剂作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni原子的核外电子排布式为_______,Ni元素位于元素周期表的第_________族。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有_________molσ键。
③某镍白铜合金的立方晶胞结构如图所示。
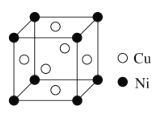
该晶体中距离Ni原子最近的Cu原子有_________个,若合金的密度为dg/cm3,阿伏加德罗常数的数值为NA,晶胞边长a=_________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组在某温度下测定溶液的pH时发现0.01mol/L 的NaOH溶液中,由水电离出的c(H+)c(OH-)=10-22,该探究小组将pH=x的H2SO4溶液与pH=y的NaOH溶液按体积比1:10混合,混合后所得溶液恰好呈中性,若x=![]() y,则x为( )
y,则x为( )
A.2B.3C.4D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+![]() CO(g)═
CO(g)═![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g)△H2
CO2(g)△H2
Fe3O4(s)+CO(g)═3Fe(s)+CO2(g)H3
Fe2O3(s)+CO(g)═2Fe(s)+3CO2(g)H4
则△H4的表达式为__________(用含△H1、△H2、△H3的代数式表示).
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
1600℃时固体物质的主要成分为__________,该温度下若测得固体混合物中m(Fe):m(O)=35:2,则FeO被CO还原为Fe的百分率为__________(设其它固体杂质中不含Fe、O元素).
(3)铁等金属可用作CO与氢气反应的催化剂.已知某种催化剂可用来催化反应CO(g)+3H2(g)CH4(g)+H2O(g)△H<0.在T℃,106Pa时将lmolCO和3molH2加入体积可变的密闭容器中.实验测得CO的体积分数x(CO)如下表:
t/min | 0 | 10 | 20 | 30 | 40 | 50 |
x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
①能判断CO(g)+3H2(g)![]() CH4(g)+H2O(g)达到平衡的是__________(填序号).
CH4(g)+H2O(g)达到平衡的是__________(填序号).
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为__________;在T℃106Pa时该反应的压强平衡常数Kp(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为__________;
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是__________,理由是__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com