
用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
A.CuSO4 B.Na2SO4 C.CuCl2 D.NaCl
B
【解析】
试题分析:A电解反应为2CuSO4+2H2O 2Cu+ O2↑+ 2H2SO4。反应一段时间后,若要使溶液恢复原状态,应该向电解后的溶液中加入适量的CuO固体。错误。B.对于Na2SO4溶液来说,电解的实质为水,所以电解后加入一定量的水可恢复原状态。正确。C.对于CuCl2 溶液来说,电解的为电解质本身。电解的方程式为CuCl2
2Cu+ O2↑+ 2H2SO4。反应一段时间后,若要使溶液恢复原状态,应该向电解后的溶液中加入适量的CuO固体。错误。B.对于Na2SO4溶液来说,电解的实质为水,所以电解后加入一定量的水可恢复原状态。正确。C.对于CuCl2 溶液来说,电解的为电解质本身。电解的方程式为CuCl2 Cu+Cl2↑。所以反应一段时间后,向剩余溶液中加入适量水不能使溶液恢复到电解前浓度。错误。D.电解的方程式为2NaCl+2H2O
Cu+Cl2↑。所以反应一段时间后,向剩余溶液中加入适量水不能使溶液恢复到电解前浓度。错误。D.电解的方程式为2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑。所以反应一段时间后,向剩余溶液中加入适量水不能使溶液恢复到电解前浓度。错误。
2NaOH+ H2↑+ Cl2↑。所以反应一段时间后,向剩余溶液中加入适量水不能使溶液恢复到电解前浓度。错误。
考点:考查不同电解质的电解的反应原理的知识。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015届浙江省宁波市八校高二上学期期末联考化学试卷(解析版) 题型:选择题
在密闭容器中存在如下反应:A (g)+3B(g) 2C(g);△H<0,某研究小组研究了只改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
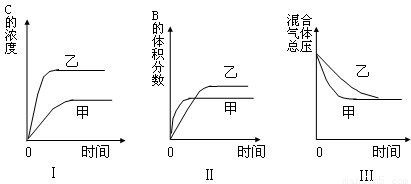
下列判断一定错误的是
A.图Ⅰ研究的是压强对反应的影响,且乙的压强较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用催化剂的效率较高
查看答案和解析>>
科目:高中化学 来源:2015届河南许昌市五校高二下学期第一次联考化学试卷(解析版) 题型:选择题
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成。下列说法正确的是( )

A.奎尼酸分子式为C9H8O4
B.1mol奎尼酸与NaOH溶液反应,最多消耗5molNaOH1mol绿原酸与Br2水反应,最多消耗6mol Br2
C.绿原酸能发生取代、加成、消去和还原反应
D.咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高二上学期期末检测化学试卷(A)(解析版) 题型:填空题
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Ag+ Na+ |
阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图。据此回答下列问题:
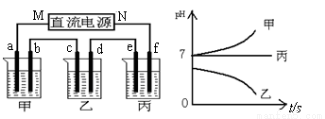
(1)M为电源的 极(填“正”或“负”),甲电解质为 (填化学式)。
(2)写出丙烧杯中反应的化学方程式 。
(3)有人设想用图一所示原电池为直流电源完成上述电解。则锌电极相当于直流电源的 (填“M”或“N”)极。
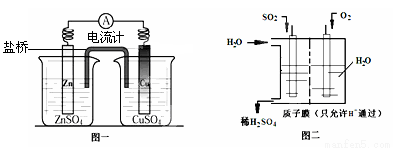
(4)有人设想用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化
为重要化工原料。该设想中负极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高二上学期期末检测化学试卷(A)(解析版) 题型:选择题
物质的量浓度都为0.1 mol·L-1的CH3COOH与NaOH溶液等体积混合后,下列关系式不正确的是
A.c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
C.c(OH-)=c(H+)+ c(CH3COOH)
D.c(CH3COOH)+ c(CH3COO-)= c(Na+)
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高二上学期期末检测化学试卷(A)(解析版) 题型:选择题
下列反应达到化学平衡后,加压或升温都能使化学平衡向逆反应方向移动的是
A.SO2(g)+NO2(g)  SO3(g)+NO(g) ΔH<0
SO3(g)+NO(g) ΔH<0
B.C(s)+CO2(g)  2CO(g) ΔH>0
2CO(g) ΔH>0
C.4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH<0
4NO(g)+6H2O(g) ΔH<0
D.H2S(g)  H2(g)+S(s) ΔH>0
H2(g)+S(s) ΔH>0
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:计算题
在体积固定的密闭容器中N2 与H2发生反应:N2(g)+3 H2 2 NH3
2 NH3
达到平衡时c (N2)=3.5 mol·L-1 ,c (H2)=1 mol·L-1 ,c (NH3)=5 mol·L-1 ,求:
(1)N2和H2的起始浓度(4分)
(2)N2的转化率(2分)(要求有解题过程)
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:选择题
在其它条件不变时,10℃时以某物质表示的反应速率为3 mol?(L· s )-1 ,已知温度每升高10℃反应速率是原来的2倍,则温度为50℃时,该反应的速率为
A.48 mol?(L· s )-1 B.36 mol?(L· s )-1
C.24 mol?(L· s )-1 D.12 mol?(L· s )-1
查看答案和解析>>
科目:高中化学 来源:2015届江西赣州市高二上学期期末联考化学试卷(解析版) 题型:选择题
已知在25℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列
有关说法正确的是( )
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.向H2S的饱和溶液中通入少量SO2气体溶液的酸性增强
C.因为H2SO4是强酸,所以反应:CuSO4十H2S=CuS↓+H2SO4不能发生
D.将足量的CuSO4溶解在0.1 mol/L的H2S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com