
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||


科目:高中化学 来源: 题型:
| 单质 | 混合物 | 氧化物 | 电解质 | |
| A | Cu | 冰水混合物 | CuO | CO2 |
| B | SO3 | Na2CO3 | 双氧水 | KOH |
| C | CH3CH2OH | 空气 | KClO3 | Mg |
| D | N2 | 浓硫酸 | H2O | FeCl3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、重金属盐能使蛋白质变性,所以误食重金属盐时,可以喝牛奶解毒 |
| B、阿胶的主要成分是蛋白质,蚕丝的主要成份是纤维素 |
| C、蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,再加水,重新溶解 |
| D、浓硝酸溅到皮肤上,会使皮肤呈现黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离的c(OH-)=10-12mol?L-1的溶液中:Br-、CO32-、K+、SO32- |
| B、含有大量AlO2-的溶液中:K+、Fe3+、Br-、SO42- |
| C、和Al反应放出氢气的溶液:Na+、Cl-、NH4+、NO3- |
| D、使pH试纸变深蓝色的溶液中:Cl-、K+、Mg2+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
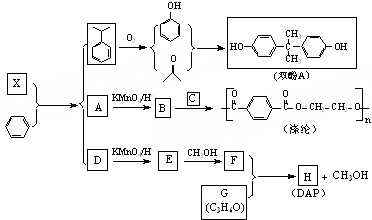
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com