
【题目】现有部分元素的性质与原子(或分子)结构如图:
元素符号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
(1)画出元素T的原子结构示意图___________。
(2)元素Y与元素Z相比,金属性较强的是_________(用元素符号表示),下列表述中
能证明这一事实的是_________(填序号)。
A、Y单质的熔点比Z单质低 B、Y的化合价比Z低
C、Y单质与水反应比Z单质剧烈 D、Y的最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性键的化合物,写出该化合物的化学式____________。
(4)元素T和氢元素以原子个数比1:1化合物形成的化合物的电子式______________。
【答案】 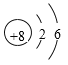 Na CD Na2O2
Na CD Na2O2 ![]()
【解析】T:最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以,次外层是K层,最外层是L层,K层排2个电子,L层排6个电子,所以是氧元素;X:由常温下单质为双原子分子,分子中含有3对共用电子对知,该元素原子最外层5个电子,主族元素的族序数=其最外层电子数,所以是氮元素;Y:由M层比K层少1个电子知,其核外电子排布是:2、8、1,所以是钠元素;Z:第3周期元素的简单离子中半径最小,由元素周期律知,金属阳离子,随原子序数的增大离子半径减小,阴离子得电子后比金属阳离子多一个电子层,都比金属离子半径大,所以是Al元素;
(1)T为氧元素,核外电子排布是2、6,原子结构示意图为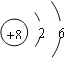 ;
;
(2)YZ分别是钠铝元素,根据元素周期律知,金属性较强的是Na,比较金属强弱的方法有:与水或酸反应的剧烈程度,其最高价氧化物的水化物的碱性强弱,金属活动性顺序表等,所以选C、D;
(3)上述元素中,由其中两种元素形成的既有离子键又有非极性共价键的物质常见的是Na2O2;
(4)氧元素与氢元素形成的原子个数比为1:1的化合物Q是H2O2.其电子式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】水法冶金技术得以迅速发展源于西汉的《淮南万毕术》中所述:“曾青得铁则化为铜”。文中涉及的化学反应类型是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学与生产、生活的认识正确的是
A. 糖类、油脂、蛋白质都可以水解
B. 石油是混合物,可通过分馏得到汽油、煤油等纯净物
C. 酸雨的pH在5.6~7.0之间
D. 新能源汽车的推广与使用,有助于减少PM2.5的产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是
A.无色溶液中:Na+、Cu2+、NO3-、Cl-
B.在pH=4的溶液中:Na+、K+、OH-、Cl-
C.在含Ba2+的溶液中:H+、Na+、Cl-、SO42-
D.与Fe反应产生气体的溶液:Na+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)为原料,制备粗铅,可以实现铅的再生利用。其工艺流程如图1所示:
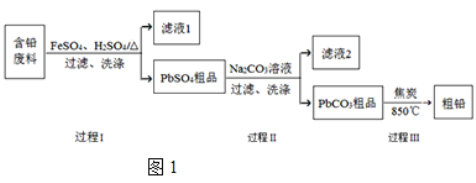
已知:Ksp(PbSO4)=1.6×105,Ksp(PbCO3)=3.3×1014。
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是 。
(2)过程Ⅰ中,Fe2+ 催化过程可表示为:
ⅰ.2Fe2++PbO2+4H++SO42==2Fe3++PbSO4+2H2O
ⅱ.……
①写出ⅱ的离子方程式 。
②下列实验方案可证实上述催化过程,将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红;b. 。
(3)过程Ⅱ的目的是脱硫。若滤液2中c(SO42)=1.6 molL1,c(CO32)=0.1 molL1,则PbCO3中____ (填“是”或“否”)混有PbSO4。
(4)为测定粗产品的纯度,可用EDTA(简写为Y4)标准溶液滴定,反应的离子方程式为:Pb2++Y4==PbY2。测定时,先称取0.2500 g粗铅,溶于足量稀硝酸,以试剂掩蔽少量干扰离子,用0.0500 mol·L1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液23.00 mL,则粗产品中铅的含量为 (以质量分数表示)。

(5)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图2所示。将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH=HPbO2+SO42+H2O。
①b与外接电源的 极相连。
②电解过程中,PbO2、PbO、HPbO2在阴极放电,其中PbO2放电的电极反应式为 。
③与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.6g铁粉投入盛有100mL 2molL﹣1稀硫酸的烧杯中,2min 时铁粉刚好溶解完全。如果反应前后溶液的体积不变,则该反应的平均速率可表示为( )
A. v(Fe)=0.5 molL﹣1min﹣1 B. v(H2SO4)=1 molL﹣1min﹣1
C. v(H2)=1 molL﹣1min﹣1 D. v(FeSO4)=0.5 molL﹣1min﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com