
从元素周期表的位置看,碳和硅均为ⅣA族元素,自然界中有碳的多种单质存在,自然界中有硅的单质吗?为什么?
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
某兴趣小组用废铁泥(主要成分为Fe2O3、FeO和少量Fe)制备磁性Fe3O4纳米材料的流程示意图如下:
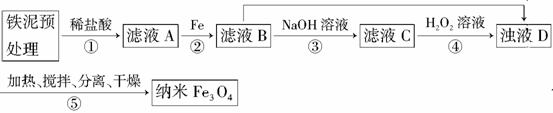
已知:R=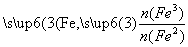 步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。
步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。
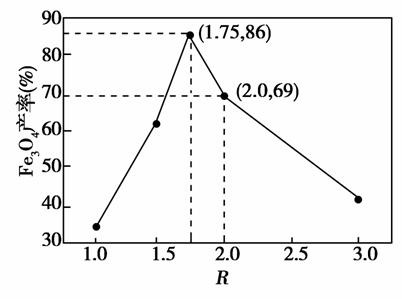
(1)步骤②中,主要反应的离子方程式是__________________。
(2)已知:Fe3+在pH=2.8时沉淀完全;Fe2+在pH=6.3时开始沉淀,在pH=8.3时沉淀完全。
步骤③中,用NaOH溶液调pH至9,原因是________________。
(3)浊液D中铁元素以FeOOH形式存在。步骤④中,反应的化学方程式是____________________。
(4)下列说法正确的是________(选填字母)。
a.步骤④中,当反应完成后需再加热一段时间
b.步骤⑤中,反应过程中需要不断补充碱液
c.步骤⑤恰好反应时,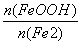 =2:1
=2:1
d.当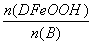 =
=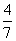 时,Fe3O4的产率最高
时,Fe3O4的产率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含
量。回答下列问题:
 ___H+ + ___MnO4- + ___H2C2O4 → ___CO2↑+___Mn2+ +____ ( )
___H+ + ___MnO4- + ___H2C2O4 → ___CO2↑+___Mn2+ +____ ( )
 (1).配平以上离子方程式,并在 ( ) 中填上所需的微粒。
(1).配平以上离子方程式,并在 ( ) 中填上所需的微粒。
 (2).该反应中的还原剂是
(2).该反应中的还原剂是
 (3).反应转移了0.4mol电子,则消耗KMnO4的物质的量为 mol。
(3).反应转移了0.4mol电子,则消耗KMnO4的物质的量为 mol。
 (4).测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
(4).测定血钙的含量的方法是:取2mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
 ①稀硫酸溶解CaC2O4沉淀的化学方程式是
①稀硫酸溶解CaC2O4沉淀的化学方程式是
 ②溶解沉淀时 (能或不能)用浓盐酸,原因是
②溶解沉淀时 (能或不能)用浓盐酸,原因是
 ③若消耗了1.0×10-4mol/L的KMnO4溶液20.00mL,则100mL该血液中含钙 g
③若消耗了1.0×10-4mol/L的KMnO4溶液20.00mL,则100mL该血液中含钙 g
查看答案和解析>>
科目:高中化学 来源: 题型:
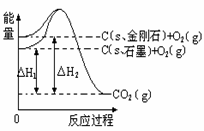
如下图所示,△H1=-393.5 kJ?mol-1,
△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是
A. C(s、石墨)== C(s、金刚石) △H= - 1.9 kJ?mol-1
B. 石墨和金刚石的转化是物理变化
C. 石墨的稳定性强于金刚石
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是元素周期表中前三周期里的四种元素,A能与D组成AD2型化合物,AD2中核外电子总数是30。离子D-的核外电子排布与Al3+相同,B和C可以形成BC型化合物,BC分子中质子总数是18,BC水溶液是一种强酸,试回答:
(1) 用电子式表示BC的形成过程:___________________________________;
(2) D单质与水反应的化学方程式是:__________________________________;
(3) 比较AD2中两种微粒的半径:r(A2+)_________r(D-)(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是 ( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊 | 饱和Na2CO3溶液 |
| B | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加入足量NaOH溶液,又变浑浊 | 澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)单质硅是将太阳能转变为电能的常用材料 ( )
(2012·新课标全国卷,8B)
(2)合成纤维和光导纤维都是新型无机非金属材料 ( )
(2012·新课标全国卷,8D)
(3)甲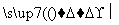 乙
乙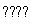 丙,若甲为焦炭,则丁可能是O2 ( )
丙,若甲为焦炭,则丁可能是O2 ( )
(2013·江苏,6A)
(4)SiO2可与HF反应,因而氢氟酸不能保存在玻璃瓶中 ( )
(2013·广东理综,10D)
(5)高温下用焦炭还原SiO2制取粗硅 ( )
(2013·广东理综,11C)
(6)SiO2有导电性,所以SiO2可用于制备光导纤维 ( )
(2012·广东理综,12B)
(7)硅酸钠溶液应保存在带玻璃塞的试剂瓶中 ( )
(2012·海南,4B)
(8)水玻璃可用于生产黏合剂和防火剂 ( )
(2010·江苏,4B)
查看答案和解析>>
科目:高中化学 来源: 题型:
氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。
Ⅰ.工业上有多种方法来制备氮化硅,下面是几种常见的方法:
方法一 直接氮化法:在1 300~1 400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为________________________________________________________________________。
方法二 化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是________________________________________________________________________。
方法三 Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体________________(填分子式);然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为____________________。
Ⅱ.(1)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,此盐中存在的化学键类型有______________。
(2)已知:25 ℃,101 kPa条件下的热化学方程式:
3Si(s)+2N2(g)===Si3N4(s) ΔH=-750.2 kJ·mol-1①
Si(s)+2Cl2(g)===SiCl4(g) ΔH=-609.6 kJ·mol-1②
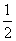 H2(g)+
H2(g)+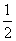 Cl2(g)===HCl(g) ΔH=-92.3 kJ·mol-1③
Cl2(g)===HCl(g) ΔH=-92.3 kJ·mol-1③
请写出四氯化硅气体与氮气、氢气反应的热化学方程式:
________________________________________________________________________。
Ⅲ.工业上制取高纯硅和四氯化硅的生产流程如下:

已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(1)原料B的主要成分是________(写名称)。
(2)写出焦炭与原料B中的主要成分反应的化学方程式:
________________________________________________________________________。
(3)上述生产流程中电解A的水溶液时,阳极材料能否用Cu?________(填“能”或“不能”)。写出Cu为阳极电解A的水溶液开始一段时间阴、阳极的电极方程式。
阳极:________;阴极________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com