
【题目】无水AlCl3可用作有机合成的催化剂,食品膨松剂等。已知AlCl3、FeCl3分别在183℃、315℃时升华,无水AlCl3遇潮湿空气即产生大量白雾。
I.工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如下:
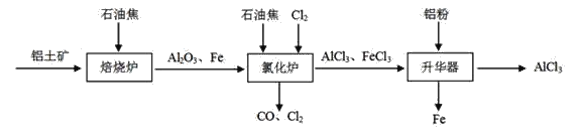
(1)焙烧炉中发生反应:①Fe2O3(s)+3C(s)![]() 2Fe(s) +3CO(g);
2Fe(s) +3CO(g);
②3CO(g)+Fe2O3(s)![]() 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
则反应②的平衡常数的表达式为K=_____。
(2)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为_____;炉气中含有大量CO和少量Cl2,可用Na2SO3溶液除去Cl2,其离子方程式为____。
(3)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%。现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g。该样品中AlCl3的质量分数为_____。
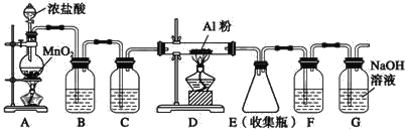
II.实验室可用下列装置制备无水AlCl3。装置B、C中应盛放的试剂名称分别为_____、_____,F中所盛放试剂的作用是_____。
【答案】K=![]() Al2O3+3Cl2+3C
Al2O3+3Cl2+3C![]() 2AlCl3+3CO SO32-+Cl2+2OH-=SO42-+2Cl-+H2O 98% 饱和食盐水 浓硫酸 防止水蒸气进入E装置
2AlCl3+3CO SO32-+Cl2+2OH-=SO42-+2Cl-+H2O 98% 饱和食盐水 浓硫酸 防止水蒸气进入E装置
【解析】
I.(1)根据反应②的方程式3CO(g)+Fe2O3(s)![]() 2Fe(s)+3CO2(g),由于Fe2O3、Fe的状态都是固体,平衡常数的表达式为K=c3(CO2)/c3(CO),故答案为:K=
2Fe(s)+3CO2(g),由于Fe2O3、Fe的状态都是固体,平衡常数的表达式为K=c3(CO2)/c3(CO),故答案为:K=![]() ;
;
(2)观察流程中氯化炉装置的物质进入和出去(看箭头指示),可以推出反应物是Fe、Al2O3、Cl2和C,生成物是AlCl3、FeCl3和CO,由此可得Al2O3、Cl2和C在高温下发生反应的产物是AlCl3和CO,反应的化学方程式为Al2O3+3Cl2+3C![]() 2AlCl3+3CO;Na2SO3溶液除去Cl2的原理是SO32-的还原性强将Cl2还原成Cl-,自身被氧化成SO42-,因SO32-水解溶液呈碱性,离子方程式为SO32-+Cl2+2OH-=SO42-+2Cl-+H2O;
2AlCl3+3CO;Na2SO3溶液除去Cl2的原理是SO32-的还原性强将Cl2还原成Cl-,自身被氧化成SO42-,因SO32-水解溶液呈碱性,离子方程式为SO32-+Cl2+2OH-=SO42-+2Cl-+H2O;
(3)AlCl3样品溶于过量的NaOH溶液后,Al元素全部转化为AlO2-进入溶液,因此过滤后的残留固体质量0.16g是样品中的杂质,AlCl3的质量分数=(16.25g-0.16g)÷16.25g=98%,故答案为:98%;
II.制备无水AlCl3,结合无水AlCl3遇潮湿空气会产生大量白雾的信息,应先制得纯净而干燥的氯气与Al反应,还要防止外界空气中的水蒸气进入装置而使AlCl3水解,由此可得装置B的作用是除去Cl2中混有的HCl,盛放饱和食盐水,装置C的作用是除去Cl2中混有的H2O,盛放浓硫酸,F中所盛放试剂的作用是防止水蒸气进入E装置而使AlCl3水解;故答案为:饱和食盐水;浓硫酸;防止水蒸气进入E装置。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】以石墨为电极分别电解水和饱和食盐水,关于两个电解池反应的说法正确的是( )
A.阳极反应式相同
B.电解结束后所得液体的pH相同
C.阴极反应式相同
D.通过相同电量时生成的气体总体积相等(同温同压)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法中正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=-2×57.3kJ·mol-1
B.101kPa时,H2的热值为142.75kJ·g-1,则表示氢气标准燃烧热的热化学方程式为:H2(g)+![]() O2(g)=H2O(l) ΔH=-142.75kJ·mol-1
O2(g)=H2O(l) ΔH=-142.75kJ·mol-1
C.由C(金刚石)=C(石墨) ΔH=-1.9kJ·mol-1可知,金刚石比石墨稳定
D.同温同压下,4Al(s)+3O2(g)=2Al2O3(s)在常温和点燃条件下的ΔH相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某传感器工作原理如图所示。利用该传感器可以测定空气中NO、CO、NH3、SO2等有害气体的含量。下列说法正确的是
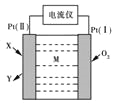
A. 传感器工作中,电子由Pt(Ⅰ)极经电流仪传到Pt(Ⅱ)极
B. 若M为熔融KOH,X为NH3,Y为N2,则负极的电极反应式为2NH3-6e- = N2+6H+
C. 若M是含O2-的固体电解质,X为NO,则正极的电极反应式为O2 + 4e- = 2O2-
D. 若X为CO,M为KOH溶液,则电池总反应为2CO+O2 = 2CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:2X(g)+Y(s)![]() Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
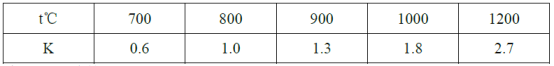
下列叙述不正确的是( )
A.上述反应的正反应是吸热反应
B.该反应的化学平衡常数表达式为K=![]()
C.若在1L的密闭容器中通入X和Y各1mol,5min后温度升高到800℃,此时测得X为0.33mol,该反应达到平衡状态
D.混合气体的密度保持不变可作为该反应达到平衡的标志之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:

步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式_________________________________。
(2)上图装置中NaOH溶液的作用是____________________________________。
(3)步骤二中,水浴加热所需仪器有____________、____________(加热、夹持仪器、石棉网除外),水浴加热的优点是_________________________________。
(4)若实验得到2.42 g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80 g固体,此样品中碱式碳酸铜的质量分数是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述不正确的是
A.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小
B.若根据反应“![]() ”设计成燃料电池,既可发电同时还可用于制备盐酸
”设计成燃料电池,既可发电同时还可用于制备盐酸
C.可逆反应的正、逆反应平衡常数数值互为倒数
D.电镀铜时,纯铜做阳极,电镀液为![]() 溶液
溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]() 。在
。在![]() 的密闭容器中进行模拟合成实验,将
的密闭容器中进行模拟合成实验,将![]() 和
和![]() 通入容器中,分别在
通入容器中,分别在![]() 和
和![]() 反应,每隔一段时间测得容器中的甲醇的浓度如下:
反应,每隔一段时间测得容器中的甲醇的浓度如下:
| 10 | 20 | 30 | 40 | 50 | 60 |
300 | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500 | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
下列说法正确的是 ![]()
![]()
A.![]() 时,开始
时,开始![]() 内
内![]() 的平均反应速率
的平均反应速率![]()
B.反应达到平衡时,两温度下CO和![]() 的转化率之比均为
的转化率之比均为![]()
C.![]() 反应达到平衡时,放出的热量为
反应达到平衡时,放出的热量为![]()
D.![]() 时,若容器的容积压缩到原来的
时,若容器的容积压缩到原来的![]() ,则
,则![]() 增大,
增大,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是

A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片始终发生析氢腐蚀
C.墨水液面回升时,正极反应式为:O2+2H2O+4e-===4OH-
D.U型管中溶液pH逐渐减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com