
| A�� | PM2.5��ָ������ֱ��С�ڻ����2.5�Ŀ����Ҳ��Ϊ����ο������ɢ�ڿ����в������γɽ��� | |
| B�� | �����г�����ʯӢ��������ͨ�������ֻ����������ڹ����β�Ʒ | |
| C�� | ʳƷ���Ӽ�����������棬������ʹ�� | |
| D�� | ���ԡ����������ֺ����ʯ��������������ʯ�ҿ�ʹ�����ʱ��Ե����� |
���� A��PM2.5��ʾÿ����������ֱ��С�ڻ����2.5�Ŀ�����ĺ�����PM2.5ֵԽ�ߣ�������ȾԽ���أ����ݽ���ֱ����PM2.5�Ĵ�С�ж���PM2.5����������Ƿ����ڽ��壻
B��ʯӢ������Ҫ�ɷ��Ƕ������裻
C��ʳƷ���Ӽ�Ӧ����ʹ�ã�
D������������ǿ�ǿ�ᡢ���¡��ؽ������ӻ���ԣ������ʾ�ʧȥ��������ԣ�
��� �⣺A��PM2.5��ָ������ֱ��С�ڻ����2.5��m�Ŀ����Ҳ��Ϊ����ο�������Կ����������ܼ��ȵ�����Ҫ��Ӱ�죮��ѧ����PM2.5��ʾÿ�������������ֿ����ĺ��������ֵԽ�ߣ��ʹ���������ȾԽ���أ�����ֱ����1-100���ף�10-9��-10-7�ף�֮�䣬PM2.5ָ��2.5��10-6�ף�PM2.5�Ĵ�С����������Χ�������γɽ��壬�������γ�������ɢϵ����A����
B��ʯӢ������Ҫ�ɷ��Ƕ������裬��������Ϊ��������ǹ����Σ���B����
C������ʹ�ù�������ʹ�õ�ʳƷ���Ӽ����������к�����C����
D����ʯ����ˮ�ᷢ����Ӧ�ų��������ȣ���������ǿ�����ʹϸ���ĵ�����ʧȥ���ԴӶ���ɱ�������ã���D��ȷ��
��ѡ��D��
���� ���⿼��ʳƷ���Ӽ��������ʵ����ʡ������κͽ��壬��Ϥ������ʵ������ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
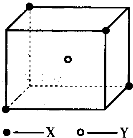 ij����ľ����ṹ��ͼ��ʾ��X��•��λ�������嶥�㣬Y����λ�����������ģ��Է�����
ij����ľ����ṹ��ͼ��ʾ��X��•��λ�������嶥�㣬Y����λ�����������ģ��Է������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | I-��ClO-��NO3-��H+ | B�� | Fe3+��Cu2+��SO42-��Cl- | ||
| C�� | H+��K+��AlO2-��HSO3- | D�� | Ca2+��Na+��SO42-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KSCN | B�� | BaCl2 | C�� | HCl | D�� | NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | t��ʱ��HA��Ka=10-2b/1000a/MV | |
| B�� | ���ʵ���Ũ�ȣ�c��HA��=1000a/MV mol•L-1 | |
| C�� | t��ʱ��HA���ܽ�ȣ�S=100a/��V g | |
| D�� | HA�������������أ�HA��=��a/��V����100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���ᷴӦFe+2H+�TFe3++H2�� | |
| B�� | �����������������ᷴӦAl��OH��3+3H+�TAl3++3H2O | |
| C�� | �ƺ���ˮ��Ӧ Na+2H2O�TNa++H2��+OH- | |
| D�� | ��������������������Һ��Al+2OH-�TAlO2-+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ̬�廯�� | B�� | ���� | C�� | �� | D�� | ������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������������ʵ���Ũ�ȵ�CH3COONH4��CH3COONa��Һ��ϣ�c��CH3COO-����c��Na+����c��NH4+����c��OH-�� | |
| B�� | ��������������ʵ���Ũ�ȵ�NH4HCO3��NaCl��Һ��ϣ���������NaHCO3��������Һ��c��H+��+c��H2CO3��=c��OH-��+c��CO32-��+c��NH3•H2O�� | |
| C�� | ����ˮ�м���NaOH��Һ��pH=7��������Һ�У�c��Na+����c��ClO-����c��Cl-����c��OH-�� | |
| D�� | ��0.10mol•L-1 Na2CO3��Һ��ͨ������CO2����Һ�У�c��OH-��=c��H+��+c��HCO3-��+2c��H2CO3�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com