
����Ŀ����ѧʵ���ǿ�ѧ̽�������е�һ����Ҫ���������ջ�ѧʵ��Ļ������������ʵ��Ʊ���ת�������ʵ�̽����Ϊ��Ҫ��������ѧ��ѧʵ��֪ʶ�ش��������⡣
I��ʵ��������220mL 1 mol��L��1��ϡH2SO4��Һ��
��1������Ͳ��ȡŨH2SO4���ܶ�Ϊ1.84g��mL��1����������Ϊ98%�������Ϊ________mL��
��2�����Ƹ���Һʱ���õ���Ҫ��������Ͳ���ձ�����������________��________�ȡ�
��3������������ʹ���ƽ��ƫ�����________��
���ܽ��δ��ȴ��ת�ơ�����
�ڶ���ʱ��������ƿ�̶���
������Ͳ��ȡһ�������Ũ����ʱ����
�ܽ���Ͳ���ձ���������ϴ��2��3�Σ�ת��������ƿ
II����ͼA��B��C��ʵ���ҳ����ļ������巢��װ�ã�

��1��ʵ���������Bװ���Ʊ��������仯ѧ����ʽ��___________________________��
��2�������Ƶø���İ�����Ӧѡ�õĸ������_______������ţ���ͬ����
����ˮCaCl2 �ڼ�ʯ�� ��Ũ���� ����ˮCuSO4
��3������Aװ����Dװ�������Ʊ����ռ�X���壬��X���������������е�_______��
��CO2 ��NO ��Cl2 ��H2
������Dװ��������С�ձ���Ŀ����________________________________��
III��ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ���������µ�ʵ��װ�á�

��1���ٷ�Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ���ֵ������ǣ�
B��_____________________________��D��________________________��
��ֹͣͨ�����ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�Ϊ
B��_____________________________��D��________________________��
��2����һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶����ǿ�����ǽ��Ƶõ�SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ���������������������������������ԭ���û�ѧ����ʽ��ʾ��_________��
��3����Eװ���п�ʼ����200mL 11.8 mol��L��1��Ũ�����������MnO2���壬��Ӧ��Ļ���ᆳ����������Һ������������AgNO3��Һ�����ó��������ʵ����ķ�ΧΪ_____________mol��
���𰸡�13.6 250mL����ƿ ��ͷ�ι� �٢� 2NH4Cl��Ca(OH)2 ![]() CaCl2��2H2O��2NH3�� �� �� ����β������ֹβ����Ⱦ���� Ʒ����ɫ Ʒ����ɫ ��ɫ��Ʒ���ָֻ��ɺ�ɫ ���������� Cl2+SO2+2H2O==2HCl+H2SO4 1.18mol��n��2.36mol
CaCl2��2H2O��2NH3�� �� �� ����β������ֹβ����Ⱦ���� Ʒ����ɫ Ʒ����ɫ ��ɫ��Ʒ���ָֻ��ɺ�ɫ ���������� Cl2+SO2+2H2O==2HCl+H2SO4 1.18mol��n��2.36mol
��������
I����1��ע��ֻ������250ml��Һ������250ml��Һ���㣻
��2����������һ�����ʵ�����Һ���裺һ���������������ת����ϴ�Ӱ˶���ҡʮװ����ȷ��ÿ��������������������⣻
��3�������ܽ��δ��ȴ��ת�ơ����ݣ�������������������
�ڶ���ʱ��������ƿ�̶��ߣ���ʹ��ˮ�Ӷ��ˣ�
������Ͳ��ȡһ�������Ũ����ʱ���ӣ���ʹ����ȡŨ�������ƫ�٣�
����Ͳ����ϴ�ӣ�ϴ�ӻ��������ƫ�࣬������ҺŨ��ƫ��
II����1��Bװ��Ӧ���ǹ�������巴Ӧ�Ʊ�����������ѡ���Ȼ�����������Ʒ�Ӧ��
��2���������ڼ������壬Ӧѡ�õļ��Ը������
��3��Aװ��Ӧ���ǹ�����Һ����ȷ�Ӧ��Һ����Һ����ȷ�Ӧ�� Dװ�ÿ��Կ�������Ӧ������Ũ�����������������ſ������ռ��������ܶȱȿ��������������Ҫβ����������ֹ��Ⱦ������
III����1����SO2����ˮ����Ư���ԣ�ʹƷ����ɫ��
��SO2Ư��������ʱ��Ư�ף�������ɫ�ָ�����ˮƯ������������Ư�ף�������ɫ���ɻָ���
��2������������������1��1ͬʱͨ�뵽��Һ�лᷢ��SO2+Cl2+2H2O=2HCl+H2SO4��Ӧ���Ӷ�ʧȥƯ���ԡ�
��3��MnO2��Ũ���ᷴӦ���������Ϊϡ����ʱ����Ӧ��ֹͣ���������м��㡣
��1��Ũ��������ʵ���Ũ��c1=![]() ������c1V1=c2V2�е�ʽ��18.4��V1��10-3=1��250��10-3���ó�V1=13.6mL��
������c1V1=c2V2�е�ʽ��18.4��V1��10-3=1��250��10-3���ó�V1=13.6mL��
��ȷ�𰸣�13.6��
��2�����Ƹ���Һʱ���õ���Ҫ��������Ͳ���ձ�����������250mL����ƿ �� ��ͷ�ιܣ�
��ȷ�𰸣�250mL����ƿ �� ��ͷ�ιܡ�
��3�����ܽ��δ��ȴ��ת�ƣ�������Һ�¶ȸ�ʱ����Ƚϴ���ɶ���ʱ��ˮ���ˣ����������ҺŨ��ƫ��
�ڶ���ʱ��������ƿ�̶��ߣ���ʹ��ˮ�Ӷ��ˣ����������ҺŨ��ƫС��
������Ͳ��ȡһ�������Ũ����ʱ���ӣ���ʹ����ȡŨ�������ƫС������ƫ�٣����������ҺŨ��ƫС��
����Ͳ����ϴ�ӣ�ϴ�ӻ��������ƫ�࣬���������ҺŨ��ƫ��
��ȷ�𰸣��٢ܡ�
II����1��Bװ��Ӧ���ǹ�������巴Ӧ�Ʊ�����������ѡ���Ȼ�����������Ʒ�Ӧ�����仯ѧ����ʽ��2NH4Cl��Ca(OH)2 ![]() CaCl2��2H2O��2NH3����
CaCl2��2H2O��2NH3����
��ȷ�𰸣�2NH4Cl��Ca(OH)2 ![]() CaCl2��2H2O��2NH3����
CaCl2��2H2O��2NH3����
��2������ˮCaCl2�백����Ӧ����CaCl28NH3 ���ڼ�ʯ�ҿ��Ը����Ũ�����백����Ӧ��������泥�����ˮCuSO4��NH3��ˮ��Ӧ����������ͭ������泥�
��ȷ�𰸣��ڡ�
��3��Aװ��Ӧ���ǹ�����Һ����ȷ�Ӧ��Һ����Һ����ȷ�Ӧ��Dװ�ÿ��Կ�������Ӧ������Ũ�������������ſ������ռ��������ܶȱȿ��������������Ҫβ����������ֹ��Ⱦ������
��CO2��ȡװ�ô����ü��Ȣ�NO������е�������Ӧ���������ſ������ռ�����Cl2�����ö���������Ũ������ȷ�Ӧ��Ũ������Ը���ܶȱȿ��������������ſ������ռ�����Һ������β������H2�ܶȱȿ���С���ռ��������ԣ�
��ȷ�𰸣��� ����β������ֹβ����Ⱦ������
III����1����SO2����ˮ����Ư���ԣ�ʹƷ����ɫ��
��ȷ�𰸣�Ʒ����ɫ Ʒ����ɫ
��SO2Ư��������ʱ��Ư�ף�������ɫ�ָ�����ˮ��Ư������������Ư�ף�������ɫ���ɻָ���
��ȷ�𰸣���ɫ��Ʒ���ָֻ��ɺ�ɫ ����������
��2������������������1��1ͬʱͨ�뵽��Һ�лᷢ��SO2+Cl2+2H2O=2HCl+H2SO4��ӦʧȥƯ���ԡ�
��ȷ�𰸣�Cl2+SO2+2H2O==2HCl+H2SO4
��3���������м��㡣
Ũ����������HCl�����ʵ���Ϊn=cV= 11.8 mol��L��1��200��10-3 L =2.36mol
�ټ�������MnO2��Ũ���ᷴӦ��Ũ���ᷴӦ��
MnO2+4HCl��Ũ��![]() MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
4 1
2.36mol 0.59mol
MnCl2+2AgNO3=2AgCl��+Mn��NO3��2
2 2
0.59mol 1.18mol
�ڼ���Ũ����û�к�MnO2��Ӧ
AgNO3 + HCl = AgCl��+ HNO3
1 1
2.36mol 2.36mol
��ΪMnO2��Ũ���ᷴӦ���������Ϊϡ����ʱ����Ӧ��ֹͣ�����������Ȼ��������ʵ���Ϊ1.18mol��n��2.36mol��
��ȷ�𰸣�1.18mol��n��2.36mol


 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��С���о��������Ļ�ԭ�ԣ��������ʵ�顣
��� | ʵ�鷽�� | ���� |
�� |
| ����a�����ɰ�ɫ������3 min�����������Ϊ���ɫ |
�� |
| ����b�����ɰ�ɫ������3 min�������ɫ�������� |
��1��ʵ�����õ�FeSO4��Һ��Fe2(SO4)3��Һ���������۷�Ӧ�Ƶã����ӷ���ʽ��____��
��2��ʵ��I�г�����Ϊ���ɫ�Ļ�ѧ����ʽ��________��
��3������ʵ��II�а�ɫ��������ɣ�С��ͬѧչ���о���
�� ��֪Fe(HCO3)2��ˮ�в����ڡ��Գ�������������¼��裬�벹��������
����a������NaHCO3��Һ��_______�ԣ��Ʋ��ɫ��������ΪFe(OH)2��
����b����ɫ��������Ϊ_______��
�� �о���ɫ������ɵ�ʵ�����£�
i��ȡ������ɫ���������ϴ�ӣ������м���ϡ���ᣬ������ȫ�ܽ⣬������ɫ���ݣ�
ii����������Һ�е���KSCN�Լ�����Һ��������죻
iii����ii��Һ���ٵ�������H2O2����Һ������Ϊ��ɫ��
�ɴ�˵������ɫ������һ������_________���ӡ�
�� �о������з��ְ�ɫ�����ڿ����о��ã����ձ�Ϊ���ɫ����ó�����ʵ��I�����õ�Fe(OH)2______����ѡ����ס����ڱ�����������
��4���Ա�ʵ��I���о�����ԶԶ�������ԭ�Ե�Ӱ�죬���ʵ��III��

��ʵ�鷽����������______��
��5��������ʵ�飬Ϊ����������������������ɲ�ȡ�Ĵ�ʩ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����200 mL ij���ʵ���Ũ�ȵ�NaOH��Һ�л���ͨ��һ������CO2 ����ַ�Ӧ�õ�Na2CO3��NaHCO3�Ļ����Һ��������������Һ�У���εμ�2 mol�ML�����ᣬ����������������������������ϵ��ͼ��ʾ��

��1��OA�Ρ�AB�η�����Ӧ�����ӷ���ʽ��_____________________��___________________��
��2��B��ʱ����Ӧ������Һ�����ʵ����ʵ���Ũ����_____________��
��3��ԭNaOH��Һ�����ʵ���Ũ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᱵ(BaTiO3)�ڹ�ҵ������Ҫ��;����Ҫ�������������մɡ�PTC�������衢�������ȶ��ֵ���Ԫ�����������������ᱵ��һ�ֹ�������ͼ:
![]()
��֪:�ٲ��������ѱ�����Ļ�ѧʽΪBaTiO(C2O4)2��4H2O��
��25��ʱ��BaCO3���ܶȻ�Ksp=2.58��10-9��
(1)BaTiO3��TiԪ�صĻ��ϼ�Ϊ:__________��
(2)���������ʱ������Ӧ�����ӷ���ʽΪ: __________��
(3)������ͨ�����˵õ����������ѱ������Ϊ��߲�Ʒ������Ծ���ϴ�ӡ�
�ٹ��˲�����ʹ�õIJ���������_____________________��
�����֤��������ϴ��?_______________________��
(4)TiO2���кܺõ�ɢ���ԣ���һ������Ҫ��;�Ľ����������ҵ�Ͽ���TiCl4ˮ�����Ʊ����Ʊ�ʱ����������ˮ��ͬʱ���ȣ���Ŀ����:_______________��
(5)ij��ȤС��ȡ19.70gBaCO3ģ���������������Ʊ�BaTiO3���ò�Ʒ13.98g��BaTiO3�IJ���Ϊ:________��
(6)�������������������ʵ����BaCO3�ܽ�ƽ����ƶ���������Һ��c(Ba2+)=0.1mol/L����c(CO32-)�ڽ���Һ�е����Ũ��Ϊ__________ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ���ǣ�������
A. �÷�Һ�ķ����������ͺ�ú��
B. ����ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿ�
C. ������������Һմ��Ƥ���ϣ�������ϡNaOH��Һ��ϴ
D. �ñ�����ˮ��ȥ���еı���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��400 ��ʱ��ij�ܱ���������X��Y��Z�������壬�ӷ�Ӧ��ʼ���ﵽƽ��ʱ������Ũ�ȵı仯��ͼ����ʾ(�ٶ���Ӧ������Ӧ�������)��ͼ��Ϊ��Ӧʱ�̽��ı䷴Ӧ��ϵ��ijһ�����������淴Ӧ������ʱ��仯�������

��1����Ӧ�ӿ�ʼ��ƽ��ʱv(X)��________________��A��B��C������淴Ӧ�����ɴ�С��˳��Ϊ_______________________________________________��
��2����t3 sʱ�ı�������ǽ���ѹǿ����Z���ʵ���ʼŨ����________��400 ��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ________��
��3��t4 sʱ�ı��������________�����÷�Ӧ�����Է��ԣ����ʱƽ����________________(��������Ӧ�����������淴Ӧ������)�ƶ���
��4����ͼ���л��Ƴ�t6 sʱ�������м���һ����X������ƽ��Ĺ�����(ѹǿ���ֲ���)�����淴Ӧ���ʵı仯���߲�ע���������͡�____________________
��5���о��������÷�Ӧ�������¼����Σ�
3X(g)![]() 2Q(s)��P(g) ��H1 Q(s)===Y(g)��W(g) ��H2 P(g)��2W(g)
2Q(s)��P(g) ��H1 Q(s)===Y(g)��W(g) ��H2 P(g)��2W(g)![]() Z(g) ��H3
Z(g) ��H3
��д��X��Y��Z�䷴Ӧ���Ȼ�ѧ����ʽ________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������зḻ��ʳƷ���������Դ��ҩ���ˮ����Դ����ͼΪ��ˮ���õIJ��ֹ��̣������й�˵����ȷ����
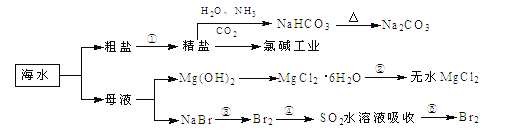
A. ��ȡNaHCO3�ķ�Ӧ���������ܽ��С��NaCl��NH4Cl
B. �ٴ����ᴿ�г�ȥ��������Mg2+��Ca2+��SO42-ʱ�������ȳ�Ca2+���SO42-
C. �ڹ������������У���Ԫ�ؾ�������
D. ��ҵ��ͨ����ⱥ��MgCl2��Һ��ȡ����þ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��µĹ̶������з�����Ӧ2SO2(g)��O2(g)![]() 2SO3(g)����Ũ����ʱ��Ĺ�ϵ���±�������˵���������(����)
2SO3(g)����Ũ����ʱ��Ĺ�ϵ���±�������˵���������(����)

A. 0 minʱ����Ӧ��������淴Ӧ����Ϊ��
B. 0��40 min�ڣ�����Ӧ���ʴ����淴Ӧ����
C. 50 minʱ�ﵽ�˻�ѧƽ�⣬��ʱ����Ӧ���ʵ����淴Ӧ����
D. 50 min���Ժ��ʱ���ڣ�������ƽ��״̬����Ӧ����������Ũ�Ȳ��ٷ����仯����Ӧֹͣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��������Һ��ˮ�ĵ���̶���С����
A. pH��11�İ�ˮ B. 0.01 mol/L��Na2CO3��Һ
C. 0.01 mol/L������ D. pH��4��NaHSO3��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com